MEDICINA |
|
|
McGovern Institute for Brain Research, MIT
El catedrático y farmacéutico Juan Carlos Izpisúa Belmonte tiene en su mano, la posibilidad de curar miles de enfermedades genéticas o por primera vez en la historia poder hablar sin fantasías de revertir el envejecimiento en términos de salud y ciencia. Vamos a conocer un poco mejor el trabajo de este investigador único que ya va camino de ser un habitual en las quinielas de los Premios Nobel.
Coincidiendo con el final de la Semana Mundial para la Concienciación de las Enfermedades Mitocondriales y las enormes implicaciones cargadas de esperanza que conlleva estas investigaciones para poder luchar contra las enfermedades de origen genético, vamos a publicar un reportaje que por fin ayude a comprender a todo el mundo la importancia de las herramientas de edición génica sobre todo CRISPR Cas9 y muy especialmente su alumno más aventajado: HITI, a través de un emocionante recorrido por la investigación de uno de nuestros mejores científicos.
Comenzaremos a principios de este mismo mes de septiembre, cuando saltaba a los medios de comunicación una vez más el equipo de científicos liderado por este profesor del Laboratorio de expresión Génica del Instituto Salk (EE. UU.) y catedrático extraordinario de Biología del Desarrollo de la UCAM (por simplificar el abultado currículo de este hombre excepcional) y anunciaba el desarrollo de una nueva técnica para curar grandes heridas regenerando la piel y sin necesidad de injertos a través de la “reprogramación celular in vivo”, un método que de tener éxito podría sustituir incluso a la cirugía plástica en muchos casos.
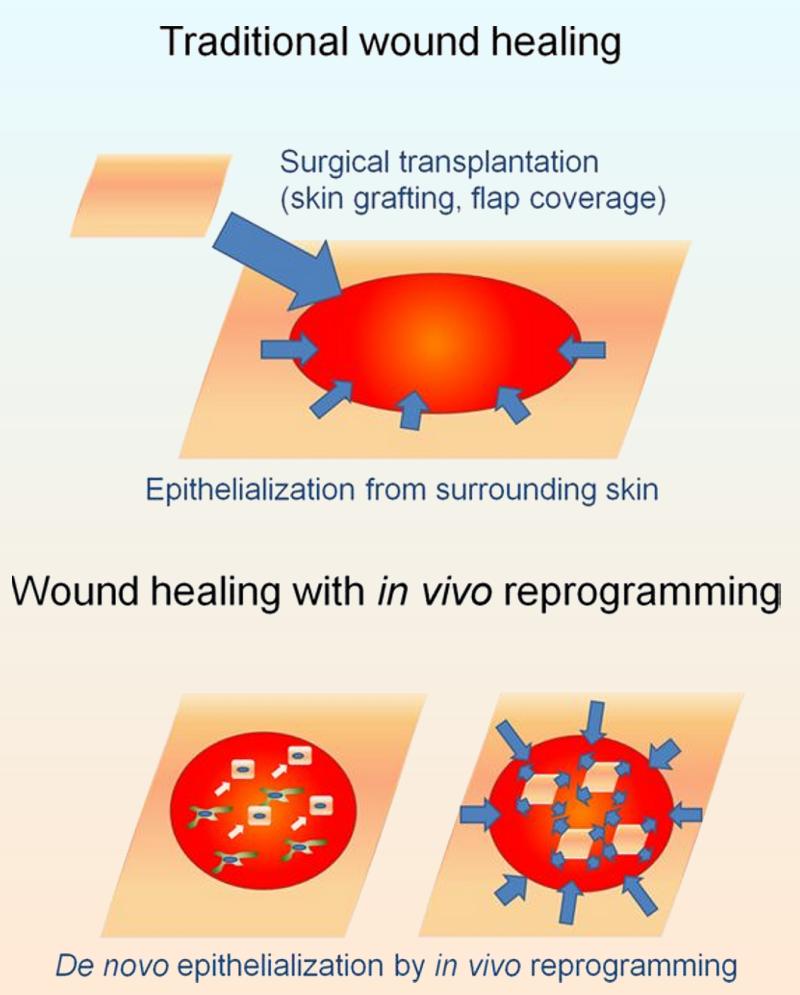
Descripción de la curación de heridas con reprogramación en vivo frente al método tradicional por trasplante quirúrgico donde se realiza un injerto de piel y se produce un proceso de epitelialización en la piel circundante. Nature/ The Salk Institute/ Kyorin University School of Medicine/ UCAM/ KAUST
El procedimiento, publicado hace unos días en la revista Nature hace historia, abriendo un tremendo abanico de futuras aplicaciones tanto para curar daños cutáneos como grandes úlceras, por ejemplo las causadas por enfermedades crónicas como la diabetes o graves quemaduras, contrarrestar los efectos del envejecimiento o ayudarnos a comprender mejor el cáncer de piel. Con el camino marcado por Francisco Mojica en la investigación de CRISPR Cas y sumando las nuevas técnicas de edición génica que Izpisúa Belmonte y su equipo están desarrollando, miles de investigadores en todo el mundo sueñan ya con infinitas posibilidades para poder manipular la genética humana con más seguridad y probabilidades de éxito para así poder tratar miles de enfermedades genéticas incurables hasta ahora o poder profundizar en la lucha de las alteraciones genéticas que conducen al cáncer o al propio envejecimiento. Lógicamente Izpisúa y su equipo todavía se muestran cautos con los resultados, como comenta su compañera Masakazu Kurita tras la reciente publicación: “Antes de ir a la clínica hay que hacer más estudios sobre la seguridad a largo plazo de este enfoque y mejorar su eficiencia” Así que este reportaje no va a tratar sobre las elucubraciones fantásticas y los sueños que el impresionante trabajo de este hombre están causando, gracias a su genial acercamiento a la genética, si no que vamos a profundizar en sus trabajos de los últimos años y sobre todo en lo más importante: el cómo, porque lo realmente interesante de Izpisúa Belmonte es el brillante intento de comprensión de la biología molecular que ha realizado y su enfoque magistral de la manipulación genética.
“Vivimos un momento revolucionario para la humanidad. Tenemos en nuestras manos técnicas, casi inimaginables hace poco, que permiten modificar animales y plantas, insectos y microorganismos. Podrían usarse para producir biofuels, para eliminar la polución, para mejorar nuestros alimentos, para mejorar nuestra capacidad de diagnóstico, para producir compuestos farmacéuticos que alteren el curso de muchas enfermedades, o, por ejemplo, para erradicar especies invasivas causantes de enfermedades que afectan a cientos de millones de personas como la fiebre amarilla, el dengue o la malaria.” Juan Carlos Izpisúa Belmonte –El Mundo, 3 Sep. 2018. Imagen: Peter Schwarz
Estrategias regenerativas “in vivo”, haciendo crecer tejido. Empecemos entonces, mirando su trabajo más reciente, un ejemplo perfecto donde se ve como Izpisúa plantea el futuro de la reprogramación genética y su utilidad práctica en cada nuevo paso que da. Cuando la gran mayoría de animales y los seres humanos nos hacemos un pequeño corte o rasguño, el organismo dispone de los medios y capacidad para reparar el daño y conseguir cerrar la herida en poco tiempo, reduciendo el riesgo de infección o pérdida de sangre, pero si la lesión adquiere mayores dimensiones, esos mecanismos dejan de funcionar con la misma eficiencia y rapidez, así que la piel no cicatriza dejándonos por ejemplo expuestos a una infección. Hasta este momento el camino para tratar las úlceras más graves en la piel consistía en trasplantar tejido cutáneo de otro lugar del cuerpo del paciente, un procedimiento que se complicaba a medida la superficie dañada era mayor. En estos casos se aislaban células madre de la piel del paciente para hacerlas crecer “in vitro”, es decir, cultivarlas en el laboratorio, para una vez alcanzado el tamaño adecuado injertarlas de nuevo. Este es un tratamiento muy largo, que obligaba a toda una serie de procesos para manipular el tejido, con el consiguiente riesgo de deterioro o contaminación de este, además que la funcionalidad y estructura de este nuevo tejido cultivado en laboratorio no era exactamente igual a su homólogo natural, por lo que en casos graves donde el tiempo es vital y factores como las infecciones juegan un papel decisivo, la vida del paciente se ponía en riesgo. Así pues, consciente del problema Izpisúa y su equipo planteó un abordaje diferente gracias al conocimiento adquirido en los últimos años en sus investigaciones, planteando acortar los plazos de tiempo y mejorar los índices de supervivencia de los pacientes a través de conseguir hacer crecer el tejido directamente en la zona afectada. Concretamente en esta investigación los científicos reconstruyeron tejido cutáneo en ratones, pero no solo eso, si no que el procedimiento, al realizarse directamente sobre la zona afectada del paciente (en este caso un ratón) consiguieron obtener una piel más natural, ya que es generada por el propio organismo y por tanto funcionalmente mejor que la producida “in vitro”.
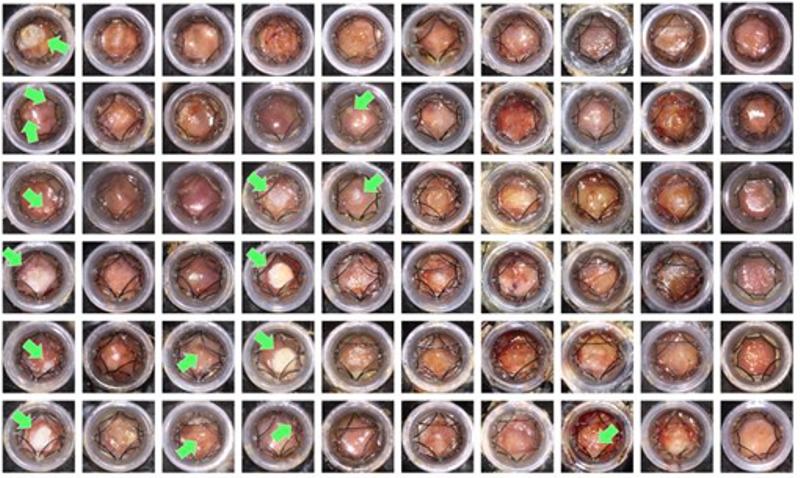
En la imagen de la investigación podemos ver diversas muestras de la reprogramación de células mesenquimales de ratón con diferentes combinaciones en la administración de DGTM-AAVs (virus adenoasociados) Nature/ The Salk Institute/ Kyorin University School of Medicine/ UCAM/ KAUST
Aplicando sus conocimientos previos obtenidos en reprogramación celular, modificando “in vivo” en la propia zona de la lesión, valiéndose de cuatro proteínas claves, reprogramaron las células del tejido conectivo en queratinocitos, ya que estas son las células predominantes de la epidermis, la capa más superficial de la piel y que contiene una proteína muy dura llamada queratina, además de producir citocinas unas moléculas con funciones de regulación de las células epiteliales y células dérmicas. Es decir estaban seleccionando las células más idóneas para generar piel directamente sobre la herida. A continuación, por medio de un virus las transmitieron de nuevo a la úlcera, consiguiendo que creciera piel nueva y funcional, en un plazo de tan solo 18 días. Como explicaba el propio Izpisua a Nature: "Nuestras observaciones constituyen una prueba de concepto para la regeneración 'in vivo' de un tejido tridimensional completo como es la piel, no sólo diferentes tipos de células aisladas como se ha hecho anteriormente" El trabajo es histórico: por primera vez se ha resuelto un abordaje que permitirá diseñar estrategias regenerativas “in vivo” para reparar tejidos “tridimensionales” con distintos tipos celulares, dicho con sencillez: un camino real para regenerar tejidos y órganos en el futuro, “sin necesidad de implantar nada externo” ofreciendo nuevas puertas al tratamiento de grandes quemados, el cáncer de piel o las consecuencias del envejecimiento y vías alternativas o complementarias de la cirugía plástica. Lo mejor es que las implicaciones aún son todavía mayores ya que tiene cabida en cualquier disciplina médica que conlleve “reemplazar a aquellos tejidos y órganos que dejan de ser funcionales por enfermedad, accidente o por envejecimiento” Anteriormente ya se había conseguido la regeneración de células individuales, como los cardiomiocitos (células del músculo cardíaco capaces de contraerse de forma espontánea e individual), pero nunca antes se había logrado formar un tejido completo en el propio organismo, siendo siempre necesario un trasplante. El equipo de investigadores observó con detalle el proceso de regeneración y curación en pequeñas heridas destacando la misión clave de los queratinocitos basales, (presentes en el estrato más profundo de la epidermis) los cuales son muy similares a las células madre y esto no era casualidad, ya que estas actúan como precursores de diferentes tipos celulares, dirigiéndose a las heridas desde el tejido sano cercano para reparar los daños. Teniendo esto presente, comenzaron ensayos de prueba-error y así los investigadores consiguieron identificar cuatro factores a través de los cuales se podía reprogramar el estado de células mesenquimales presentes en la herida hasta convertirlas en queratinocitos basales, que poco a poco fueron generando piel hasta curar la herida. Las células madre mesenquimales (CMM) son un ejemplo de células madre de tejido o madre “adultas”, son células multipotentes, o sea que pueden dar lugar a más de un tipo de célula especializada del cuerpo, pero no a todos los tipos. Algunos estudios iniciales sugerían que las CMM también podrían dar lugar a varios tipos de células diferentes que no pertenecían al tejido esquelético, como células nerviosas, células del músculo cardíaco, células hepáticas y células endoteliales, sin embargo, durante mucho tiempo estos resultados no fueron confirmados por estudios posteriores. Sin embargo, el equipo de Izpisúa lo consiguió y además, tras reprogramarlas y comenzar el crecimiento, no fue necesario ningún tipo de andamiaje previo para guiar a las células en el proceso de crecimiento y distribución, si no que como señaló el propio Izpisúa, “Las células reprogramadas tenían una capacidad innata para crear piel nueva hasta que la lesión se cerró”, dejando de crecer por sí mismas cuando no quedaba rastro de la herida, algo que sucedió a los 18 días.
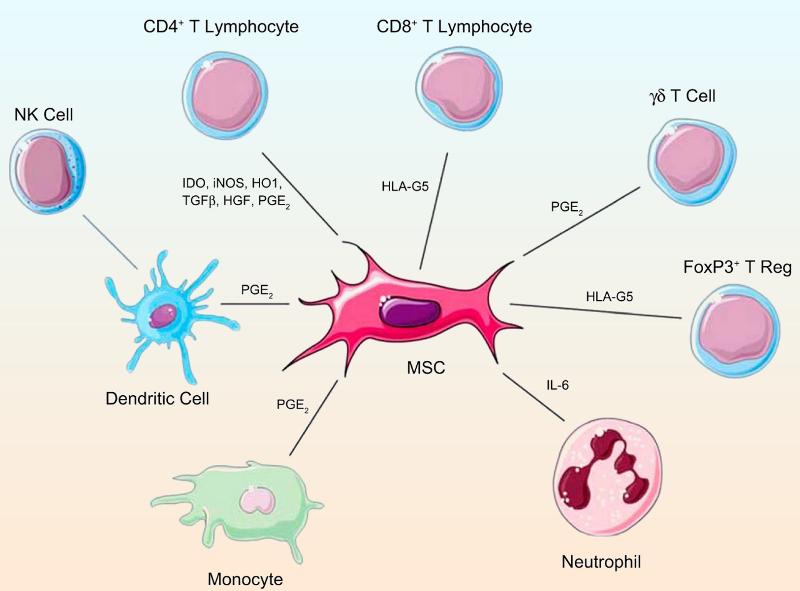
Las células madre mesenquimales (MSC) Las MSC pueden formar una variedad de tipos de células en el laboratorio, incluyendo las del linaje intray extra mesenquimal. Estos tipos de células incluyen: grasa (adipocitos), hueso (osteoblastos), piel (células dérmicas), nervio (células neurales), cartílago (condrocitos), músculo (miocitos esqueléticos), tendones (tenocitos), estroma de la médula ósea, ligamentos y más. tienen ventajas sobre otros tipos de células madre por una variedad de razones. Evitan los problemas éticos que rodean a la investigación con células madre embrionarias, repetidos estudios han encontrado que las MSC son inmuno-privilegiadas y son de un gran interés terapéutico, ya que representan una población de células con potencial para tratar una amplia gama de enfermedades agudas y degenerativas. Stem Cell Training
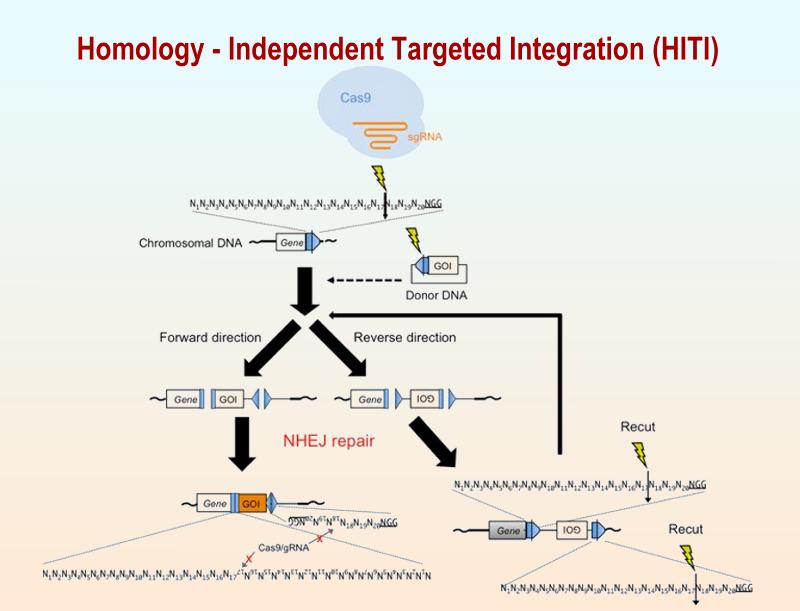
Este último detalle es bastante relevante, pues en la investigación con ratones no se observó ningún crecimiento celular descontrolado ni alteraciones relacionadas con la administración de los factores de reprogramación, es decir con el virus que se utilizó como vehículo para transportar los citado queratinocitos, como ocurre por ejemplo con el crecimiento descontrolado en un cáncer. Aunque claro, es muy importante asegurarse que el proceso es fiable a largo plazo antes de iniciar ensayos con seres humanos, lo que conlleva que los científicos también continuarán optimizando el procedimiento, así como su eficacia en otros modelos animales, antes que en seres humanos, pero si los estudios llegan a buen puerto se abre la puerta a intentar aplicarlo en la regeneración de órganos. ¿Interesante verdad? Ahora retrocedamos un poco en el tiempo para viajar por el trabajo de Izpisúa y su equipo, que ya comienza a ser un habitual en los medios de comunicación no especializados por sus espectaculares hallazgos y comprendamos de una vez que son estos novedosos procedimientos. HITI el alumno aventajado de CRISPR Comenzaremos en noviembre de 2016 de la mano de este gran científico y su equipo, (que por cierto incluye otros grandes investigadores españoles), en esa época llegaba a los medios de comunicación una nueva técnica de edición genética, llamada a cambiar la historia, su nombre: HITI. Por primera vez el equipo dirigido por Izpisúa Belmonte del Salk Institute había logrado alcanzar una localización concreta de las células adultas que no se dividen, es decir ya incapaces por sí solas de regenerar tejidos u órganos y modificar su ADN dañado. El resultado del trabajo publicado de nuevo en la prestigiosa Nature y firmado además por científicos del Hospital Clínic de Barcelona, la Universidad Católica de Murcia y la Clínica Cemtro de Madrid, marcaba la consolidación de esta nueva técnica que mejoraba a distancia todo lo existente hasta ese momento. Hasta ese momento, las técnicas existentes para editar genomas de manera sencilla y precisa en el ADN de seres vivos, como el sistema CRISPR-Cas9, habían sido más eficaces en células en división, como podrían ser las de la piel o el intestino, la novedad de la nueva técnica es que se aplicaba por primera vez en células que no se dividen.
Nature / Keiichiro Suzuki & Juan Carlos Izpisua Belmonte
Este es un detalle de suma importancia porque las células que no tienen la capacidad de dividirse, cuando enferman no tienen posibilidad de regenerarse. Este fue el caso de la enfermedad tratada en ratones: retinitis pigmentosa, una enfermedad que provoca la destrucción progresiva de las células del epitelio pigmentario de la retina provocando un estrechamiento del campo de visión hasta dejarlo al mínimo. Los investigadores, valiéndose de la nueva técnica “insertaron” ADN en una posición concreta del genoma de estas células que no se pueden ya dividir, así que por primera vez en la historia, conseguían “cortar” la parte del gen dañado y “pegar” un gen con la información correcta, lo que a la práctica significaba que la célula enferma se curaba, logrando reparar parcialmente la ceguera de los ratones.
En este ameno vídeo publicado por el propio Instituto Salk se explica de una manera muy sencilla la nueva tecnología de edición génica basada en CRISPR/Cas9 - Salk Institute for Biological Studies
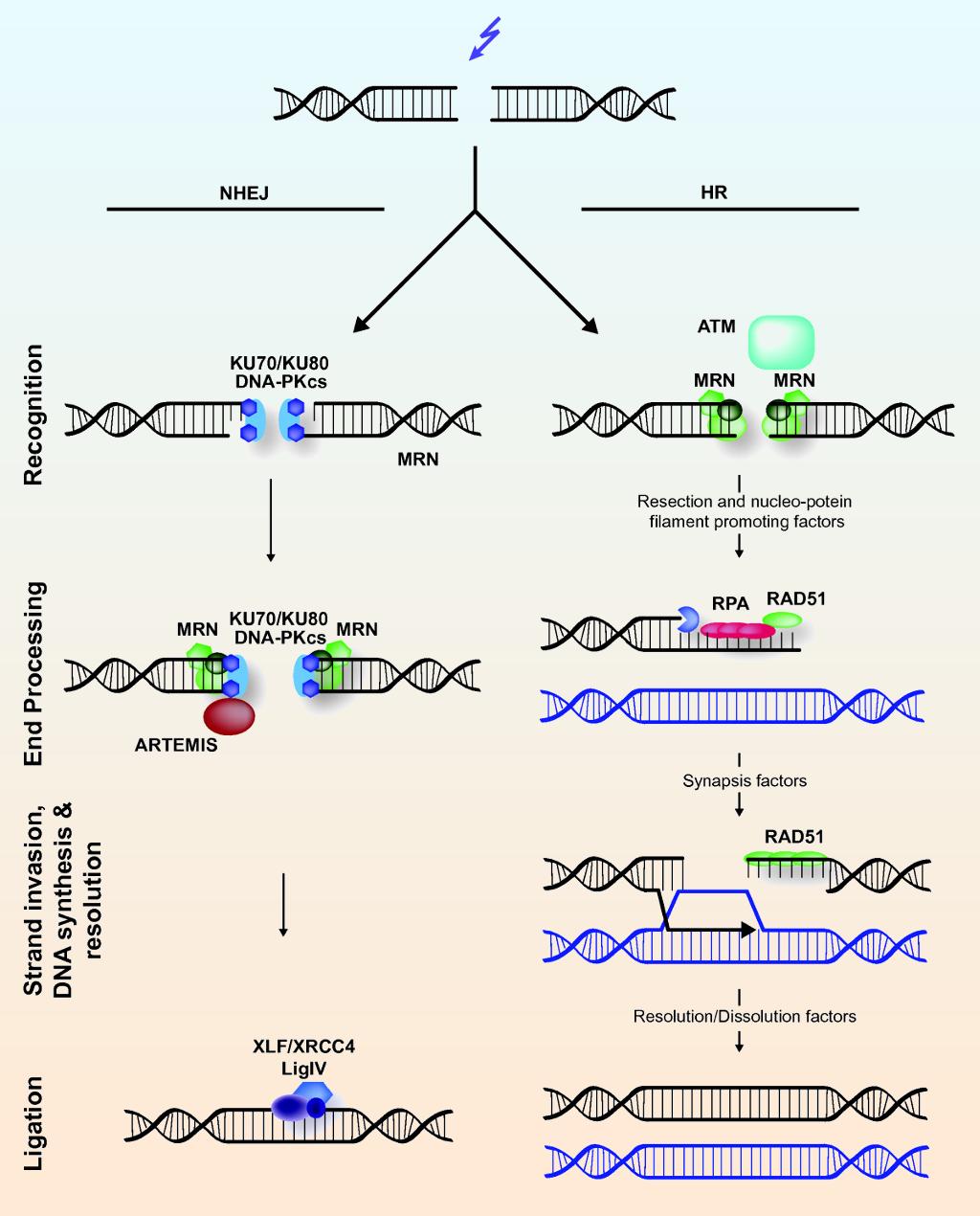
NHEJ Para lograr su objetivo los investigadores enfocaron sus objetivos en una vía celular de reparación del ADN llamada: unión de extremos no homólogos (NHEJ), -Non homologous end joining en ingles - era una vía revolucionaria para insertar ADN que permitía la edición del genoma en organismos adultos vivos y que nadie había hecho antes (luego lo explicaremos con más profundidad). Los investigadores tuvieron que optimizar la maquinaria NHEJ para su uso con la técnica Crispr-Cas9, para ello el equipo creó un paquete de inserción personalizado compuesto por un conjunto de ácidos nucleicos al que denominaron HITI (Homology-Independent Targeted Insertion). Una vez puesto a punto, utilizaron un virus inerte para entregar el paquete de instrucciones genéticas de HITI en células derivadas de células madre embrionarias. Lo que se había logrado era casi revolucionario, pues el éxito no radicaba tanto en curar la retinitis pigmentosa (no fue una elección al azar, ni mucho menos, se comenzó precisamente por esta enfermedad ya que era una dolencia muy estudiada y por tanto un buen modelo para investigar), sino en la propia técnica de edición génica, ya que ofrecía un sin fin de nuevas vías para la investigación básica y también el desarrollo de una gran variedad de tratamientos de patologías de base genética de la retina, neurológicas o cardíacas por ejemplo.
Unión de extremos no homólogos (NHEJ) y recombinación homóloga (HR) en mamíferos por roturas en la doble cadena de ADN DSB ((Double strand DNA breaks) Hannes Lans, Jurgen A Marteijn and Wim Vermeulen - BioMed Central
Cuando se presentó la nueva tecnología hace dos años se ofrecía ya como al menos diez veces más eficiente que otros métodos preexistentes para editar y poder incorporar nuevo ADN, demostrando que se podía introducir fragmentos de ADN dentro del genoma humano, por lo que se abrían casi infinitas posibilidades para tratar también enfermedades de otros órganos tales como el riñón, corazón, cerebro o el sistema musculo-esquelético. Solo con esto ya podríamos hablar de un punto y aparte en la historia, pero además los horizontes terapéuticos llegaban mucho más lejos porque esta innovadora tecnología abría nuevas vías para el tratamiento de enfermedades monogénicas, es decir aquellas producidas por alteraciones en la secuencia de ADN de un solo gen. Y esto último es realmente importante, pues como sabemos nuestros genes sirven de patrón para la producción de diferentes proteínas y juntos proporcionan la información necesaria para definir cualquier elemento de nuestro organismo y sus funciones. Cuando tan solo uno de ellos es erróneo, puede producir una proteína anormal o en cantidades anormales que altere estas funciones. Aunque no siempre los rasgos anormales que heredamos provocan consecuencias para la salud o son mínimas, también pueden producir en otras ocasiones alteraciones que lleven a una disminución importante en la calidad de vida o incluso la muerte. Así pues las enfermedades hereditarias afectan al 1-2% de la población general, existen muchísimas sin tratamientos efectivos a día de hoy, cuando la prevalencia es baja o son enfermedades raras (recordemos las enfermedades mitocondriales que recordamos esta semana), el problema para tratarlas y disponer de medicación adecuada es mucho mayor, por lo que la nueva técnica representaba todo un avance sin precedentes para tratar miles de enfermedades genéticas que antes no se podían curar. Claves en la epigenética, ratones y la lucha contra el envejecimiento El comienzo del año 2017 resultó de nuevo un momento emocionante para la medicina y la genética, poco después del nuevo año ya se hablaba de las investigaciones sobre revertir el envejecimiento que le dieron fama internacional fuera de su entorno, cuando consiguió alargar la vida de ratones gracias a la reprogramación celular y hacer soñar a los más optimistas, aunque la cosa no es tan sencilla, lo podemos garantizar. Por entonces, junto al habitual equipo científico del Instituto Salk consiguieron aumentar la esperanza de vida en ratones con una enfermedad genética conocida como progeria, desde una media de 18 semanas a 24.
Ratones con progeria tratados por los investigadores. Salk Institute
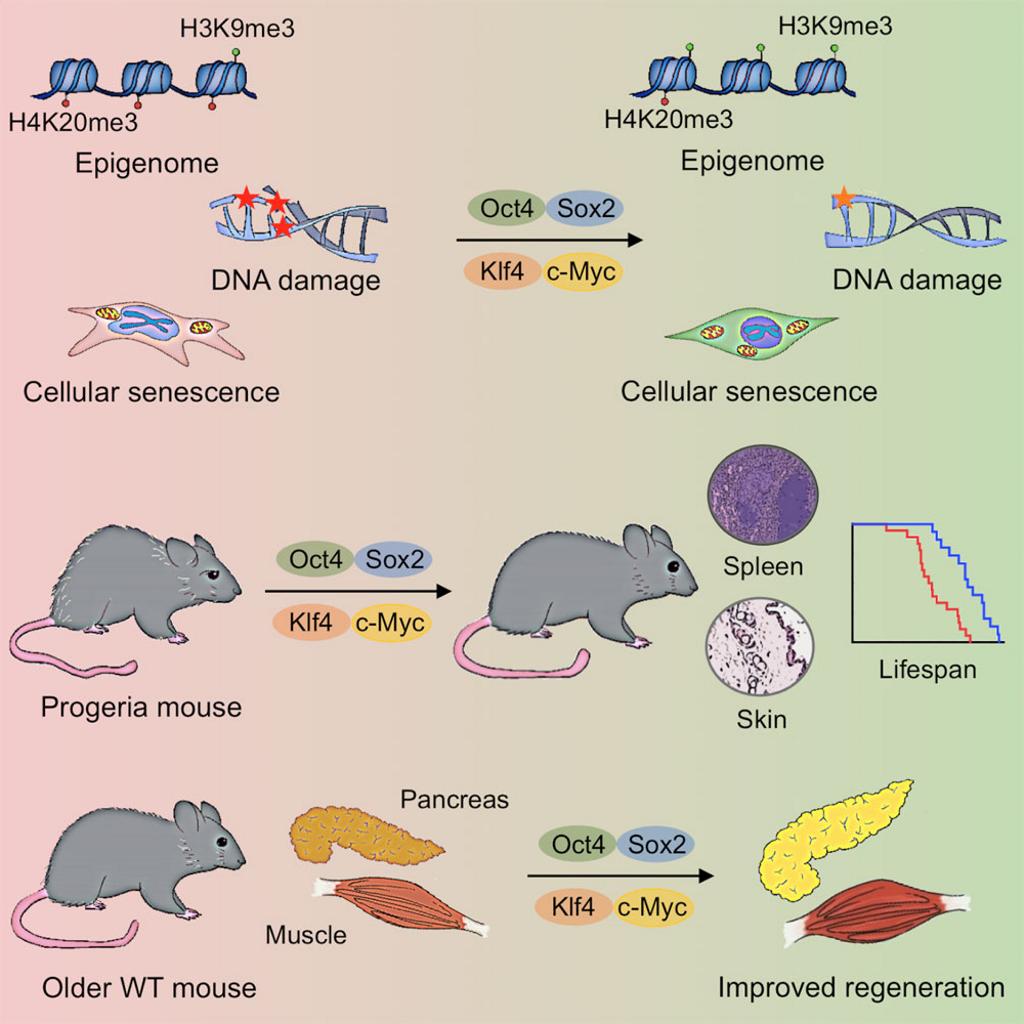
Aunque la noticia se vendió por los medios de comunicación como que se había conseguido encontrar la manera de alargar la vida de los ratones, no era así exactamente, la progeria es una enfermedad genética que provoca el envejecimiento prematuro, así que corregir el defecto solo suponía en apariencia alargar en torno un 30% más la vida de los ratones, unas 6 semanas. ¿No parece muy espectacular, verdad? Sin embargo lo es y mucho, pero debemos verlo desde un punto de vista diferente: Los investigadores habían conseguido revertir los signos del envejecimiento prematuro en estos ratones afectados de progeria a través de la reprogramación de marcas epigenéticas, marcas químicas que se añaden al material genético y permiten su correcta actividad. ¡Aquí está la clave! El planteamiento parte de que dichas marcas, que controlan la expresión de los genes y protegen nuestro ADN, pueden ser manipulables, llegando incluso a reducir las consecuencias negativas, así pues Izpisúa y su equipo no había corregido la mutación que causa la progeria en los ratones, es decir la mutación que les causaba el envejecimiento prematuro, sino que alteraron el envejecimiento cambiando el epigenoma, lo cual tiene implicaciones enormes ya que parece demostrar que ciertos procesos biológicos son así alterables, en este caso el envejecimiento o como el propio Izpisúa dice: flexibles. Aquella investigación otra vez marcó un hito histórico realmente importante, era la primera vez que en un estudio se conseguía prolongar la vida de un animal vivo a través de la manipulación del epigenoma, pues los anteriores trabajos por estas vías acabaron con ratones muertos o con tumores.
Esquema del tratamiento de ratones afectados de progeria a través de la reprogramación de marcas epigenéticas, Salk Institute
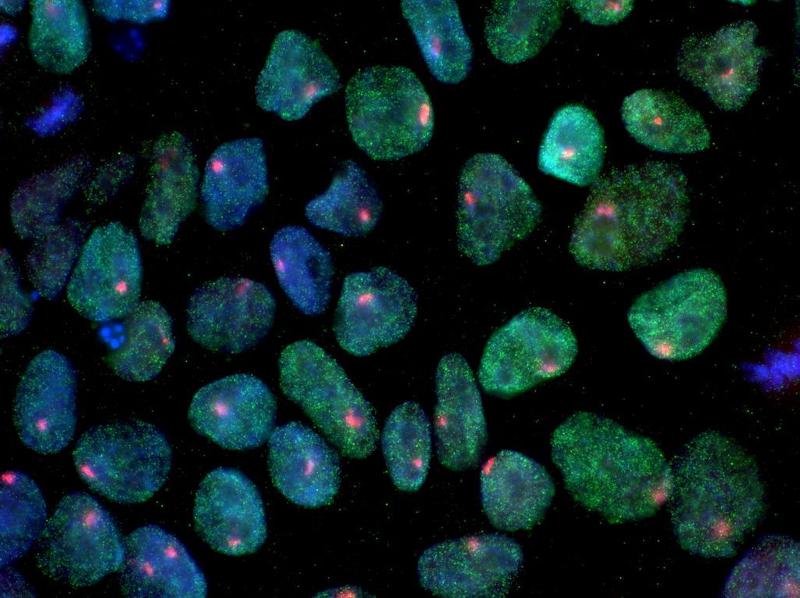
Las células de la piel usadas en el estudio rejuvenecían por cambios epigenéticos, aunque en aquel momento no sabían mucho sobre cuáles eran exactamente las marcas y los cambios responsables de este proceso de envejecimiento, pero desde entonces Izpisúa ha seguido aprendiendo más sobre cómo cambia el epigenoma durante la reprogramación parcial y así poder desarrollar nuevos métodos para revertir estos cambios de una manera más específica y optimizada, es decir: "Convertir completamente un programa epigenético viejo en uno joven", como el mismo indica. iPS y reprogramación parcial Antes de seguir y para poder hablar con propiedad sobre esta materia debemos tener muy claro que es una célula pluripotente inducida, así pues, la reprogramación celular de la que estamos hablando convierte células adultas en células pluripotentes inducidas (iPS), o sea que tengan una elevada tasa de proliferación y todavía no estén especializadas para la realización de funciones específicas. Para poder trabajar con ellas, es decir reprogramarlas, se requiere inducir la expresión de cuatro factores en estas células, conocidos como factores Yamanaka (así conocidos en honor a su descubridor, el premio Nobel Shinya Yamanaka del que hablaremos más adelante). Los factores mencionados deben expresarse durante un periodo de 2 a 3 semanas para que las células adultas alcancen la pluripotencia, pero en el caso de esta investigación, el equipo de Izpisúa utilizó la reprogramación parcial, lo cual significa que indujo la expresión de los “factores de Yamanaka” durante un periodo de tan solo 2 a 4 días. Así consiguieron un curioso objetivo: las células reprogramadas no alcanzaban la pluripotencia, sino que continuaban manteniendo su especificidad anterior, lo cual significaba que no perdían su identidad, es decir, continuaban manteniendo la función a la cual estaban destinadas antes de la reprogramación, pero eran capaces de dividirse indefinidamente, como las embrionarias y así detener los signos de la vejez, con lo que los roedores tratados con este procedimiento parecían más jóvenes, su función cardiovascular había mejorado, el tejido de la piel, el bazo, el riñón o el estómago tenían un aspecto renovado ya que se consiguió disminuir la acumulación de daño en el ADN y restaurar la estructura nuclear, deteriorada por el paso del tiempo y los factores externos en las citadas células.
Células madre pluripotentes inducidas a partir de las células de la piel. Kathrin Plath Labs, University of California, L.A.
El objetivo final comenzó a definirse claramente: no era solo lograr que vivamos más (algo claramente limitado por la evolución y sus reglas, completamente alejadas de nuestros sueños de inmortalidad) sino que vivamos más años sanos y con mayor calidad de vida, ya que reduciríamos el riesgo de padecer muchas enfermedades y afrontaríamos los tratamientos con una nueva perspectiva. El “salto” ya estaba listo, pero… ¿De qué va el salto? La carrera ya había comenzado, los investigadores del Instituto Salk habían empleado con éxito el sistema CRISPR-Cas9 y su novedosa herramienta HITI para tratar diversas enfermedades en ratones sin necesidad de alterar su ADN, demostrando más allá de cualquier logro hasta ese momento que disponíamos de un “bisturí molecular” viable que podía “encender” y “apagar” los interruptores que controlan nuestro genoma sin modificar el ADN. Aunque no era la primera vez que se borraban mutaciones sin alterar el ADN, el enfoque del grupo de Izpisúa era pionero al hacer que la edición genómica “in vivo” actuara sobre los interruptores que regulan la expresión de nuestros genes. Se había demostrado que era factible alterar el fenotipo de un animal, o sea, el conjunto de características visibles que lo caracterizan, mediante una tecnología que editaba el epigenoma, preservando de forma simultánea la integridad del ADN.
De izquierda a derecha: Jun Wu, Reyna Hernandez-Benitez, Keiichiro Suzuki y Juan Carlos Izpisua Salk Institute
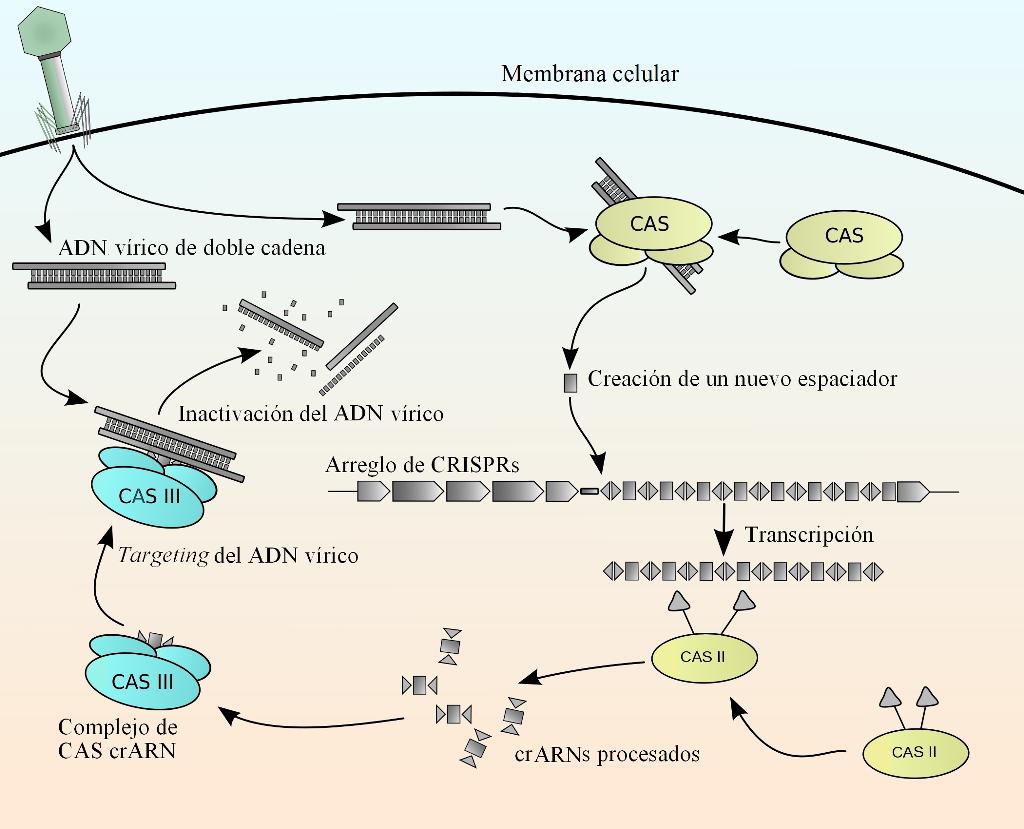
De funcionar correctamente Izpisúa y sus compañeros habían diseñado una nueva técnica que lograba corregir mutaciones asociadas a patologías como la diabetes, la insuficiencia aguda de riñón y la distrofia muscular en modelos animales actuando sobre los marcadores epigenéticos, ahora tocaba acercarse al borde del trampolín y dar el salto. Como funciona CRISPR-Cas 9 Antes de llegar al “salto” que se produjo en 2017, si lo que estamos contando a despertado vuestro interés, será mejor detenerse un momento y conocer un poco mejor el funcionamiento del sistema que lo revolucionó todo y su evolución. Cuando hablamos del sistema CRISPR-Cas realmente nos referimos a un mecanismo de inmunidad adaptativa que presentan las bacterias para defenderse del ataque de los virus y que estudió con detenimiento el investigador alicantino Francisco Mojica pionero en esta materia. Si un virus intenta infectar a un microorganismo, este activa una especie de sistema de backup para guardar un fragmento del genoma del virus en su propio ADN. Parece una respuesta extraña pero tiene mucho sentido: si el agresor vuelve a agredir a la bacteria, el microorganismo tendrá la capacidad de “activar” el procedimientio CRISPR-Cas y actuar como un bisturí a nivel molecular sobre el material genético y cortar el virus para frenar su ataque. Este mecanismo en las formas de vida más elemental fue descubierto hace ya tres décadas y supuso como sabemos una revolución que ha permitido a lo largo de los últimos años continuar investigando en esta importante función biológica donde las bacterias puedan defenderse del ataque de un virus. Pero es solo a partir de 2012 que damos el gran salto, gracias a las investigaciones realizadas por Jennifer Doudnar al comienzo, seguidas por las de Feng Zhang y George Church después ofreciendo nuevas aplicaciones para el sistema CRISPR-Cas. Poco a poco los científicos fueron cayendo en la cuenta de que este potente bisturí prometía impresionantes posibilidades para editar tanto el genoma en bacterias como en células de mamíferos y por supuesto, de los seres humanos, ya que al fin y al cabo, no lo olvidemos, el “diccionario de la vida” se escribe igual para todos los seres vivos, del más grande a una bacteria.
Posible mecanismo de los CRISPR (clustered regularly interspaced short palindromic repeats: repeticiones palindrómicas cortas agrupadas y regularmente interespaciadas) Estos son familias de secuencias de ADN en bacterias que contienen fragmentos de ADN de virus que han atacado a las bacterias y que estas utilizam para detectar y destruir el ADN de nuevos ataques de virus similares, jugando un papel clave en los sistemas de defensa bacterianos. Expresándonos con más precisión diremos que son loci de ADN que contienen repeticiones cortas de secuencias de bases. Tras cada repetición siguen segmentos cortos de "ADN espaciador" proveniente de exposiciones previas a un virus. Con frecuencia estos se hallan asociados con los genes cas, que codifican para proteínas nucleasas relacionadas con los CRISPR, formando el sistema CRISPR/Cas, un sistema inmunitario procariótico que confiere resistencia a agentes y provee una forma de inmunidad adquirida. Los espaciadores de los CRISPR reconocen secuencias específicas y guían a las nucleasas cas para cortar y degradar esos elementos génicos exógenos de una manera análoga al ARNi en sistemas eucarióticos – Roddelgado/ Wikimedia
Había nacido pues, una nueva era para el desarrollo de posibles terapias génicas y vías inexploradas para resolver miles de enfermedades sin cura o difíciles de tratar con un acercamiento completamente novedoso y prometedor. Ya sabemos a groso modo como funciona: es un bisturí capaz de cortar las dos hebras del ADN, pero una vez hemos realizado el corte donde nos convenga… habrá que re-pegar ¿no?
Roturas, roturas y más roturas
Durante la vida de las células, su ADN puede deteriorarse, bueno, lo cierto es que es lo normal, puesto que está sometido a muchos ciclos de replicación y división, sin mencionar los agentes externos. Algunos estudios calculan que una persona que llegue a los 70 años, por término medio, habrá sufrido 2.000 roturas de su ADN en sus distintas células (algunos estudios ponen el asunto peor, pero dejemos ahí las cifras) Estas roturas en la doble cadena, en ocasiones con pérdidas incluso en ambos extremos, donde se produce una pérdida de fragmentos de nucleótidos en los mismos, las llamamos DSB (Double strand DNA breaks) Cuando estos fallos ocurren, el propio ADN tiene mecanismos para intentar repararlos, genes que se traducen en proteínas actuando como ADN-polimerasas de reparación que intentan solucionar los daños, así como otras proteínas que actúan de factores de transcripción de los anteriores, trabajando en equipo según sea el tipo de rotura producida, a esto lo podríamos llamar a groso modo: el kit de copiado. Para esta labor existen varios tipos de ADN-polimerasas de reparación según el daño causado, además como si habláramos de pegamento estarían las ligasas para sellar la reparación efectuada. Si hablamos de sólo una hebra del ADN la que se ha roto, entonces sería una SSBRR (Single strand break repair). Es en principio el problema más sencillo de solucionar para una célula. La otra hebra o cadena, (elijan el nombre que más les guste) actuará de molde para que las proteínas anteriormente mencionadas, unas actuando como enzimas y las otras realizando un complejo proteico de reparación, retiren los nucleótidos dañados de herida y coloquen los nucleótidos complementarios según están dispuestos en la otra cadena complementaria que todavía está intacta y les proporciona la información adecuada Pero si la rotura es más compleja entonces la reparación se complica… ¡y puede complicarse demasiado! Puede ser incluso una rotura de la doble cadena, aquí el asunto ya es mucho más grave puesto que se puede perder la continuidad del ADN (aconsejo fijarse en el símil con las antiguas tarjetas informáticas perforadas que se menciona un poco más adelante), por si fuera poco, a menudo sus extremos se pueden deshilachar, (el paralelismo con unos hilos trenzados no es exactamente igual, pero nos puede dar una idea muy aproximada) así que pueden producirse pérdidas de algunos nucleótidos en los extremos, con la consiguiente pérdida de información.
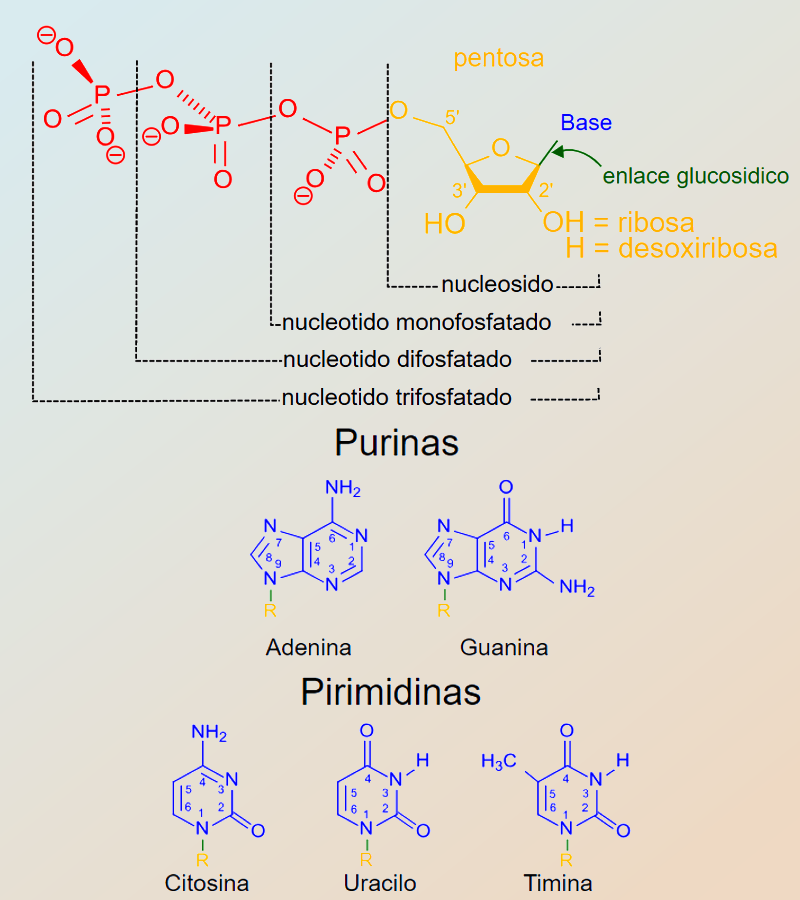
Un pequeño apunte para los más nuevos en la materia, acabamos de mencionar los nucleótidos, pues bien nuestro ARN y el ADN son polímeros formados por largas cadenas de nucleótidos. Un nucleótido a su vez está formado por una molécula de azúcar (ribosa en el ARN o desoxirribosa en el ADN) unido a un grupo fosfato y una base nitrogenada. Las bases utilizadas en el ADN son la adenina (A), citosina (C), guanina (G) y timina (T) y son estas cuatro bases las que componen todas las letras con las que escribimos el libro de la vida, es decir, la información contenida en nuestro ADN y ARN. En la imagen podemos ver los elementos estructurales de los nucleótidos más comunes.
Cuando ocurre esto la mecánica de la vida puede recurrir a 2 tipos de reparación, en función del momento y de la magnitud de la rotura: El primero es lo que llamamos: la unión de extremos no homólogos, denominada NHEJ (es el camino empleado por Izpisúa que mencionamos anteriormente) con esta vía, nuestras propias células pegan los trozos cortados, esto sería el proceso más asimilable a si se tratase de una herida. Pero esta vía tiene sus problemas, exactamente igual que cuando nos provocamos un buen corte en la piel por ejemplo, ya que este mecanismo provoca cicatrices en nuestro material genético y puede producir inserciones o deleciones de genes. Eso quiere decir que en esos bordes aparecerá información no deseada o desaparecerá contenido necesario para el correcto funcionamiento del organismo… y eso puede ser un serio problema, porque podemos estar inventando involuntariamente instrucciones que generen sustancias nocivas, eliminando funciones necesarias para el correcto funcionamiento de un órgano o simplemente cualquier cosa que sea posible escribir en la enciclopedia de la vida, sea buena o no. La gravedad del problema dependerá mucho de cómo hayan quedado los extremos rotos. Si es una rotura sin pérdida de nucleótidos en alguno de los 4 extremos (recordemos 2 hebras x 2 extremos= 4 extremos), se limpian el daño otros y se rellena con los nucleótidos correspondientes. ¡Pero cuidado!, No siempre ocurre así y puede suceder que la célula no sepa qué camino tomar para reparar el daño, en ese caso continuará limpiando eliminando nucleótidos en los extremos hasta encontrar una microhomología en las cadenas, o sea, seguirá eliminando información que no sabe interpretar químicamente como reparar hasta llegar a uno o varios nucleótidos complementarios que pueda enlazar y poder pegar la unión. El problema radica en que en algunos casos es una solución chapucera ¿Por qué? Digamos que actúa una polimerasa descontrolada que pone nucleótidos al azar. Al menos cumple su misión de mantener la continuidad de la doble cadena, pero en muchas ocasiones se pierden algunos nucleótidos de la secuencia (a esto lo llamamos una deleción). Por suerte para nosotros, una deleción no tiene por qué ser un fallo irresoluble durante la reparación, eso dependerá del lugar de la cadena de ADN donde se haya producido en que se ha producido y no tenga mayor trascendencia fisiológica, ya que el ADN a su vez se divide en según su función en varios tipos: ADN codificante, regulador o ADN “nulo o basura”, en este último caso por ejemplo las consecuencias probablemente serán nulas. ¡Banzai!
Realmente la apoptosis es un mecanismo celular extraordinariamente complejo, descrito por Kerr, Wyllie y Currie en1972. Las investigaciones científicas realizadas desde entonces, demuestran que la existencia de la apoptosis, es una necesidad celular por dos principales razones:
Primera, durante la vida de cualquier organismo, es necesario deshacerse de ciertas estructuras celulares y crear otras, es decir, mueren células y se generan nuevas, reconstruyendo estructuras en los tejidos u órganos. Segunda: Es necesario la eliminación de ciertas células que han sufrido daño, como el ocasionado por los radicales libres, cuando están infectadas por virus o bacterias, y cuando las células ha sufrido daño en su ADN. A pesar de que es un proceso ordenado, si éste pierde el equilibrio, se pierde el orden y se producen diversas patologías como malformaciones, defectos en el desarrollo, enfermedades autoinmunes, enfermedades neurodegenerativas o aparición de tumores. biocompare Pero si a pesar de la reparación llevada a cabo, el daño en la secuencia de nucleótidos es grave, podría significar un trastorno o disfunción terrible, incluso fatal para la fisiología celular. Cuando todo parece perdido, por suerte la célula tiene otro mecanismo para resolver el problema: quitarse de en medio, efectivamente: suicidarse, a esto lo llamamos apoptosis. Es un proceso por el cual la propia célula, consciente del fracaso en la reparación, envía una señal a los lisosomas (unos orgánulos relativamente grandes, normalmente encargados de la digestión celular) para que suelten su contenido digestivo/degradador de enzimas proteolíticos en el interior de la propia célula acabando con ella y desintegrándola, aprovechando sus restos las células sanas circundantes como alimento. Reparando con “molde” Tenemos una segunda posibilidad: la recombinación homóloga, con este sistema se introducen una secuencia de ADN como si fuera una “tirita” o quizás mejor dicho, un “puentecito molecular” para cerrar la herida provocada y así incorporar dicha secuencia en el lugar del fragmento de ADN que se cortó previamente. Esto es necesario y muy importante, porque el ADN es una línea de código secuencial muy, pero que muy precisa. Imaginemos una de las antiguas tarjetas perforadas con las que se programaba un ordenador de los años 60. Introducíamos esas tarjetas para cargar un programa en el ordenador y que lo ejecutara, si por alguna razón se rompía un solo fragmento de la cartulina, el ordenador comenzaba a cargar mal la información y como un programa es un conjunto de acciones aquello dejaba de funcionar correctamente y según la importancia de la parte del código afectado por la rotura de la tarjeta, aquello podía transformarse en un desastre. La única solución era reparar la tarjeta de disponer de los medios, cortando en un punto lógico y colocando bien el mismo código exactamente en el mismo lugar u otro nuevo pero solo exactamente donde comenzaba una nueva instrucción o juego de ellas y solo hasta el punto donde acabara y comenzara otra nueva. Por supuesto, respetando siempre el lenguaje y normas de la programación, de lo contrario el ordenador sería incapaz de entender las nuevas instrucciones. A este sistema lo podemos considerar una reparación con “molde” donde este es proporcionado por el ADN del otro cromosoma homólogo, por tanto sería un mecanismo muy parecido a la reparación de la rotura de una hebra: cortar el fallo, limpiar los extremos y colocar los nucleótidos a imagen de la otra hebra que actúa de plantilla. En la biología natural (si se permite la expresión) esto puede ocurrir durante el proceso de división celular, donde las fibras cromatínicas de ADN y posteriormente cromosomas están sometidas a las tensiones y desplazamientos del proceso. Por suerte los elementos homólogos acostumbran a situarse en las proximidades unos de otros, haciendo más fácil la reparación y que pueda completarse con éxito.
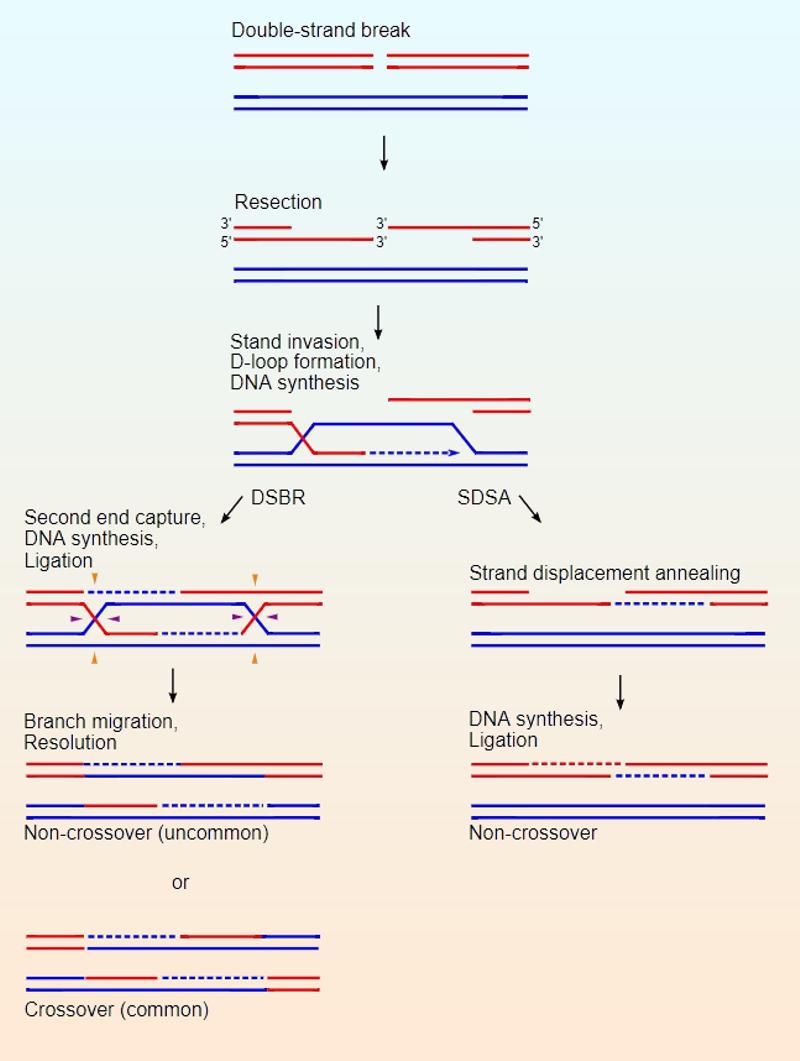
Hay dos modelos principales para la forma en que la recombinación homóloga repara las rupturas de doble cadena en el ADN son la vía de reparación de la ruptura de cadena doble (DSBR) (a veces llamado el modelo de doble cruce Holliday) y la vía de síntesis que depende de la línea del recocido (SDSA). Si bien las dos vías siguen los mismos pasos iniciales, posteriormente divergen. La vía DSBR resulta frecuentemente en entrecruzamiento cromosomal (abajo a la izquierda), mientras que la SDSA siempre termina en productos no entrecruzados (abajo a la derecha). Emw2012
Ahora que hemos aclarado todo esto un poquito mejor volvamos a los experimentos de edición génica¨: Como decíamos, los experimentos realizados para comprobar la efectividad de CRISPR-Cas9 habían utilizado normalmente el segundo mecanismo, ya que el objetivo, al igual que en nuestra antigua tarjeta perforada de cartón consistía en cortar la zona defectuosa del ADN para pegar con un trocito de celo que no alterase la secuencia genética lógica, la información molecular de ADN que corregía la mutación y así eliminar el defecto. Y aquí llegamos a una de las técnicas ideadas por Izpisúa, basada en el uso de dos virus adenoasociados (AAV), con la misión de encapsular las herramientas para editar el epigenoma e introducirlas en ratones recién nacidos. Pues bien en algunas de las investigaciones, uno de los virus sirvió para empaquetar el gen que codifica Cas9, o sea, el famoso “bisturí” que generalmente se emplea para cortar las dos hebras de ADN, aunque en este caso concreto no haya sido necesario. Luego, en el segundo virus, introdujeron la guía de ARN, que actúa como una especie de guía para dirigir el 'bisturí molecular'. Pero a diferencia de los 20 nucleótidos que suelen presentar la mayor parte de guías de ARN empleadas en los sistemas CRISPR-Cas diseñados hasta la fecha, esta nueva secuencia de ácido ribonucleico cuenta con tan solo 14-15 nucleótidos. ¿Y porqué menos nucleótidos? ¡Pues aquí está lo bueno!: Normalmente el objetivo sería precisamente que la 'mano' guiara al bisturí hacia la secuencia diana en el genoma para que una vez allí, ¡la proteína Cas9 no pueda cortar!, ya que el objetivo es precisamente actuar sobre el epigenoma (los interruptores que encienden y apagan la expresión génica) y así no modificar el ADN. Luego para poder poner en marcha la actividad en la región de ADN que tenían como objetivo, añadieron al segundo virus una proteína que trabaja como activador transcripcional. ¿El resultado de todo esto?, (es la razón de toda la explicación previa, si no estábamos muy familiarizados con la materia): al evitar la modificación del ADN, se reduce el riesgo de introducir mutaciones que podrían ser dañinas e incontrolables, que podrían llevar por ejemplo a un cáncer o la apoptosis.
Aquí os dejamos un video donde se explica la tecnología CRISPR-Cas y sus aplicaciones – Addgene / Feng Zhang's lab at MIT/BROAD institute
La herramienta de CRISPR-Cas, formada por un “equipo guía” y un “bisturí” a nivel molecular, suele emplearse para cortar una determinada región del genoma y luego repararla para introducir una mutación beneficiosa o corregir un defecto genético, pero el equipo de Izpisúa modificó el funcionamiento de este procedimiento, para no cortar las dos hebras de ADN, sino que simplemente encendiera la expresión de un gen que pudiera sernos útil . Ahora con el nuevo sistema se abría un nuevo y revolucionaria metodología que permitía activar cualquier tipo de gen o de ruta genética a través de este el sistema compuesto por CRISPR Cas9, la guía de ARN y la proteína que activa la transcripción, sin el peligro de introducir mutaciones potencialmente dañinas. Una vez diseñado el nuevo sistema basado en CRISPR-Cas para editar el genoma, el equipo de Izpisúa comenzó probar la nueva estrategia en modelos animales para saber si la herramienta molecular funcionaba in vivo y ofrecía la suficientemente seguridad y eficacia para emplearse en un futuro como una terapia en medicina. A partir de ese momento comenzaron los éxitos, la técnica era capaz de activar genes dañados o silenciados en ratones que recuperaban su función normal. También demostraron por ejemplo la utilidad del editor epigenómico para transformar células funcionales de un tipo a otro como por ejemplo de células hepáticas en pancreáticas que produjeran insulina. Hasta ahora todo los datos muestran que la técnica es segura y eficaz en ratones, aunque todavía estaba lejos de ser aplicada en la práctica clínica pero el camino quedaba abierto y comenzaron a acercase al trampolín… Luego continuaron experimentando y activaron la expresión de genes relacionados con el crecimiento y el funcionamiento de los músculos, para esquivar los daños producidos por una mutación relacionada con la distrofia muscular, lo que permitió a los ratones experimentar cierta mejoría, no una cura total, pues la mutación está todavía ahí, ya que lo que se abordaba era el epigenoma y los ratones recuperaban la expresión de otros genes de la misma ruta, cual era suficiente para restaurar la función muscular de los animales.
En este video del Instituto Salk, Juan Carlos Izpisúa de una manera didáctica como se corrigió por primera vez la mutación causante de la miocardiopatía hipertrófica en embriones humanos durante la etapa inicial. Salk Institute for Biological Studies
Esta nueva vía, de nuevo abría un abanico de futuras posibilidades ya que con ella podría estudiarse para intentar recuperar grupos de neuronas dañadas en pacientes con alzhéimer y párkinson, y por tanto una posible terapia experimental para estas enfermedades neurodegenerativas. En definitiva la genialidad probablemente no radica en sí, en cada tecnología utilizada, ya que estas eran conocidas por la comunidad científica, lo realmente innovador es su uso combinado en un único procedimiento ajustado y mejorado. Mutaciones “off-target” Luchando con el gran problema del la mutación no deseada Las técnicas con CRISPR-Cas en las que se modifica el ADN tienen un serio problema que hemos explicado: La reparación del corte es lo que conlleva la mutación (mediante inserciones y deleciones) o si se ofrece al ADN un “molde”, la edición de la secuencia. Por supuesto ese corte puede repararse de muchas maneras, pero esto genera una seria incertidumbre, pues todavía no podemos controlar con precisión la reparación del corte que realiza el “bisturí molecular” y a veces el sistema CRISPR-Cas9 puede modificar otros lugares del genoma que no querríamos y llegaríamos a las temidas mutaciones off-target. Esto obligó a los científicos a buscar nuevas estrategias para tratar de aplicar algún día la edición genómica en la práctica clínica y desde luego una de las aproximaciones que probablemente alcancen el éxito primero podría ser sin dudad la presentada hoy por el equipo de Izpisúa, a la que además podrían unirse otras ideas como el empleo de proteínas Cas9 inactivas los “bisturís” de edición que a la hora de la verdad realmente no actúan y por tanto, no modifican el ADN. Saltando del trampolín: reparación de una mutación genética en embriones humanos Y por fin llegamos a Julio de 2017, un equipo internacional de científicos, incluyendo EEUU, China y Corea del Sur presentaban junto a Izpisúa Belmonte en la revista Nature una forma eficiente de usar la herramienta de corta-pega genético CRISPR Cas9 para corregir en embriones humanos con la mutación del MYBPC3, el cual está asociado a la miocardiopatía hipertrófica, una enfermedad hereditaria que afecta a aproximadamente a una persona de cada 500 y que es tristemente conocida por causar la muerte súbita en deportistas jóvenes. Era otro momento histórico, heredar una sola copia de la mutación en el gen MYBPC3 podía significar en el desarrollo de esta dolencia, donde los tratamientos actuales tan solo alivian sus síntomas, pero no abordan la causa genética detrás de todo... contando que se han identificado más de 10.000 alteraciones hereditarias controladas por un solo gen, era una noticia excepcional. Para realizar las pruebas el equipo trato in vitro 142 embriones humanos en estados iniciales de desarrollo aunque nunca los llegaron a implantar. Inicialmente comenzaron con 167 óvulos donados por mujeres sanas que luego intentaron fertilizar con el esperma de un solo donante: un hombre portador de una mutación heterocigótica en el citado gen, o sea, con una copia mutada dominante y otra correcta.
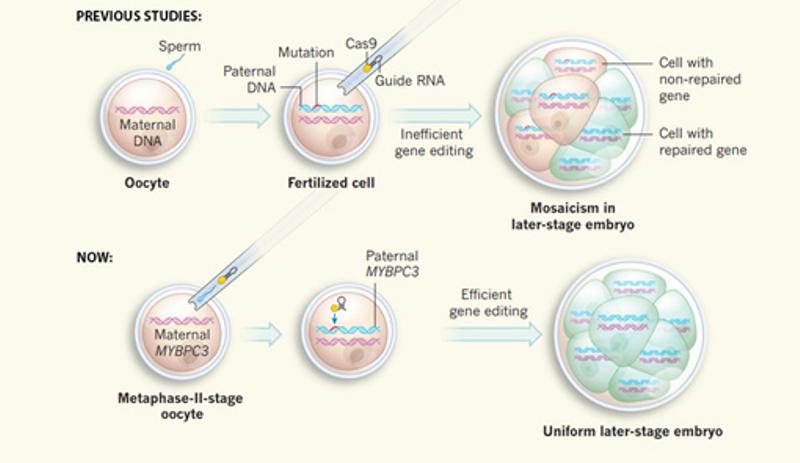
En estudios anteriores primero se fertilizaba el óvulo con el esperma y luego se añadían los componentes de edición genética, pero ahora se inyectan a la vez que el esperma, con resultados más eficientes y sin mosaicismo. Nerges Winblad & Fredrik Lanner/ Nature
Así consiguieron fertilizar los 142, con lo cual se esperaría que un 50% de los ovocitos fecundados estuvieran libres de la mutación, pero al aplicar la nueva técnica a una parte de los embriones ese porcentaje se elevó significativamente, logrando cortar la secuencia del gen mutante y observando cómo los embriones humanos eran capaces de reparar bien el ADN. Una de las observaciones más interesantes y menos esperada resulto en que, en la mayoría de los casos, las roturas se repararon de forma exitosa utilizando la propia copia no mutada del gen del donante, en vez de emplear como plantilla un ADN sintético y así consiguió que más de dos tercios de los embriones objetivo contuvieran las dos copias libres de errores del gen. En experimentos anteriores ya se había intentado usar la tecnología CRISPR para tratar enfermedades en embriones humanos, pero falló al aparecer lo que se denomina “mosaicismo”, embriones formados por células de dos o más tipos genéticamente diferentes. Como citó el propio Izpisúa: “La principal contribución de nuestro estudio ha sido desarrollar una estrategia para evitar el mosaicismo y hacer que los efectos fuera del objetivo marcado sean despreciables, gracias a la inyección conjunta del esperma y los componentes de edición genética (en oocitos no fecundados en la denominada fase M)”. (En los trabajos anteriores los componentes CRISPR-Cas9 se añadían en una etapa posterior, cuando ya estaba fertilizado el oocito). En resumen, el equipo internacional liderado esta vez por el investigador Shoukhrat Mitalipov del Centro de Células Embrionarias y Terapia Génica de la Oregon Health & Science University (OHSU, en Estados Unidos) había eliminado la variante del gen del linaje familiar y todo apuntaba a la seguridad y eficiencia de la corrección efectuada en el gen MYBPC3 abriendo por fin las puertas a una nueva era médica, donde ya existía un ejemplo “real” pero brindando ciertas garantías con respecto a las preocupaciones que existen sobre la seguridad de estos procedimientos. El nuevo sistema se podría aplicar potencialmente para corregir las miles de alteraciones genéticas que afectan a millones de personas en todo el mundo, sin transmitirlas a sus descendientes o aumentar el éxito de la fecundación in vitro al incrementar el número de embriones sanos, reduciendo el número de ciclos necesarios para las personas que intentan tener hijos libres de enfermedades genéticas. Aunque las consideraciones éticas para trasladar esta tecnología a ensayos clínicos son complejas y merecen un compromiso público importante, (por ejemplo este experimento en concreto hubiera sido ilegal en países como España), la puerta quedaba abierta y lo importante es comprender que ya hemos “saltado del trampolín” y lo importante es aprender y madurar como sociedad para limitar únicamente las actuaciones perniciosas que pudieran derivarse de poder alterar los genes humanos, pero potenciar todas aquellas que pudieran beneficiarnos y librar de enfermedades a millones de personas que hasta ahora no disponen de una cura. Juan Carlos Izpisúa Belmonte, el hombre modesto
No es un político, un gran empresario visionario, ni el escritor de moda en la ciencia ficción, si no uno de los grandes investigadores de la historia. Su nombre es ya un habitual para el premio Nobel, que con certeza recibirá antes o después, pero nació en España, en una familia humilde de Hellín (Albacete) en el año 1960 para más señas y ahora dirige el laboratorio de expresión génica del Instituto Salk de La Jolla (California) donde ocupa la cátedra del premio Nobel Roger Guillemin.
Verán, normalmente los hombres y mujeres que a lo largo de cada ciclo histórico representan la esencia de lo mejor que podemos lograr como especie rara vez son conocidos y puestos como el ejemplo en su época por el gran público. Estamos demasiado ocupados en seguir las andanzas de aquellos personajes destinados a entretenernos bajo los focos de la superficialidad, promesas vacías o esa riqueza con la que jamás se puede comprar la eternidad, así que desconocemos a los verdaderos artífices que ofrecen la oportunidad de un mañana mejor. Hoy hemos hablado de uno de ellos con la esperanza de que esto cambie, Izpisúa es un hombre único, empeñado en entender racionalmente la naturaleza, pero capaz de ver la compatibilidad entre ciencia y Dios en el amor y la ayuda desinteresada a nuestros semejantes. Pero lo dicho hace un momento no son solo palabras, Izpisúa siempre que puede reclama el apoyo de los gobiernos y la sociedad para la investigación de enfermedades incurables y hace lo que puede por buscar soluciones, embarcándose en proyectos de gran dificultad y complejidad donde otros abandonarían,( como es por ejemplo el caso de Mencía una pequeña que padece una enfermedad extremadamente rara y degenerativa). Siempre ha considerado con sabiduría que la investigación debería ser “una de las prioridades de nuestros gobernantes, como así se entiende en muchos otros países” defendiendo siempre que puede la necesidad de esta y sus virtudes. Ser uno de los científicos más reputados del mundo nunca le ha quitado humildad y honestidad, cuando se le pregunta sobre la inmortalidad, responde: “Debemos pensar en términos de salud, no de inmortalidad. En la última etapa de nuestra vida, nuestro cuerpo decae y no podemos evitarlo. El objetivo es que esos últimos años sean de mejor calidad, que la enfermedad tarde en aparecer o no aparezca.” Pero si alguna respuesta le define sería la que da cuando le preguntan por el Nobel: “¿El Nobel? No creo que lo merezca. Son premios para personas que han hecho cosas para cambiar el mundo. Mi ambición es solo ayudar a paliar enfermedades” No se me ocurre mejor manera de cerrar este reportaje, en este domingo que finaliza la Semana de Concienciación sobre las Enfermedades Mitocondriales, donde este hombre excepcional y todos los científicos que luchan en el campo de la investigación ofrecen una gota de esperanza mientras nuestras vidas pasan sin dar normalmente mucha importancia a lo que realmente importa.
Te puede interesar:
Autor: Inflexion Point Doctor
Temas relacionados: Enfermedades Raras, Investigación Médica, Biomedicina, Medicina, Pastillitas de Ciencia, Inflexion Point Doctor
Reconocimientos y más información sobre la obra gráfica
ADVERTENCIA: En este foro, no se admitirán por ninguna razón el lenguaje soez y las descalificaciones de ningún tipo. Se valorará ante todo la buena educación y el rigor sobre el tema a tratar, así que nos enorgullece reconocer que rechazaremos cualquier comentario fuera de lugar.
15 Comentarios
Moisés Garrido
26/9/2018 00:09:17
Felicidades por este tremendo reportaje, había leído hace unos días sobre este investigador y no tenía ni idea de la importancia de su trabajo, ni de las variantes en la técnicas de manipulación genética. Me ha sabido a poco, por favor IPD le agradecería un monográfico sobre CRISPR Cas9, HITI y otras técnicas empleando ese sistema único que tiene de explicar todo para "tontos"como yo. Le sigo por Facebook y adoro sus explicaciones sobre ciencia (también sus críticas ácidas a la ignorancia y la pseudociencias) sería una gozada que realizara un monográfico sobre genética parecido al que realizó sobre dolor crónico o la enfermedades metabólicas.
Responder
Inflexion Point
28/9/2018 15:02:20
Muchísimas gracias Moisés, vaya veo que tengo un fan! Guauu!!! ja,ja ...si, suelo ser muy sarcástico y agresivo con los que prometen curaciones mágicas por Intenert, en fin llevo ya un tiempo trabajando en un reportaje de introducción a la genética que sea realmente útil (dentro de mis limitados conocimientos) y otro sobre HITI y las enfermedades mitocondriales, pero hacer algo realmente completo y que todo el mundo pueda comprender, es realmente un trabajo de chinos (creo que he soltado un chascarillo políticamente incorrecto...) en fin, además estos días me encuentro de viaje por cuestiones de trabajo dando vueltas por el mundo (de ahí la tardanza en contestarles, disculpen todos). Los medios de comunicación generalistas acostumbran a centrarse más en los titulares espectaculares, la vida de esta gente o hacernos soñar con futuras pastillas para la inmortalidad, pero es lógico y les perdono, están sumidos en una crisis profunda y solo buscan poder vender rápidamente publicidad para ir tirando (creo que con esto le contesto a otras preguntas que me ha realizado anteriormente). Así que un pelín de paciencia, escribir bien sobre esto para que todo el mundo lo puedo comprender "a tope" es realmente muy difícil y cada trabajo para que salga bien lleva su tiempo, mucho tiempo pero le garantizo que estoy en ello.
Responder
Elisa S. B.
26/9/2018 10:42:35
Me apunto 100% a la petición del señor Garrido: reportaje sobre genética con su sello carácteristico para ya, mejor para ayer ¿Cuantos años faltan realmente para que se nos pueda tratar a nivel celular? Por lo que veo, prácticamente todo es con animales,¿ Cuanto tiempo falta realmente? Se agradecería profundizara en genética. Felicidades por su esfuerzo en preocuparse por tratar estos temas de unaanera diferente.
Responder
28/9/2018 15:17:55
Hola Elisa, muchísimas gracias por tus ánimos. Como le he dicho a Moisés estoy trabajando en ello hace un tiempo, pero es algo complejo, paciencia please...
Responder
Neurona apática P. G.
26/9/2018 14:31:03
Enhorabuena, yo también aplaudo la idea de un trabajo a fondo para explicar como funciona la edición de ADN, por encima del periodismo actual, que no tienen ni idea de lo que dicen, aunque le sugiero incida en las "mutaciones OFF TARGET" pues todo se pinta muy bonito, pero el riesgo a largo plazo en humanos está sin comprobar y lo que le menciono (ya he visto que lo ha citado) tiene mucho que ver y rara vez se profundiza cuando se habla de esto a la población. Gracias de antemano y siga por este camino tan poco habitual de no tratar a la población media como ignorantes.
Responder
28/9/2018 15:26:24
Gracias... P.G. (no creo que seas una neuro tan apática ;-) ). Como ya he contestado anteriormente, ya llevo un tiempo trabajando en un reportaje al respecto, es algo complicado, si realmente, como usted dice quiero tratar con el respeto que se merece a las "neuronas de la población media". Una vez más paciencia, que prometo estar en ello. Efectivamente, tiene toda la razón, las mutaciones no deseadas y la ausencia de complicaciones no deseadas por fallos en la manipulación en el ADN a largo plazo que garanticen procedimientos seguros a largo plazo son el gran misterio a resolver, para ello, como le decía a Elísa, hace falta mucho tiempo y dinero, la fase con animales previa es esencial para poder seguir, pero desde luego creo que en mis próximos reportajes incidiré mucho en este punto y en la importancia de que nos tomemos muy en serio apoyar estos proyectos para acelerar los resultados en lo posible, como ya he comentado muchas veces hay en juego el futuro de millones de vidas, algunas en estos momentos con el reloj con la cuenta atras, Un abrazo P.G.
Responder
MigueLore1
26/9/2018 23:58:06
Como menciona Neurona Apática, queds un largo camino por recorrer, el grave problema de editar el genoma son las mutaciones Off Target en otras zonas, un simple kit de CRISPR no supera los 200 dólares pero el nivel de mutaciones inesperadas que se obtiene es tremendo y cada día se demuestra mayor, el empleo de modelos de edición mejorados es una opción y plantear intervenir a través de la epigenetica es una buena idea al existir un intrusismo menor, pero al fin y al cabo esto es una batalla contra reloj entre laboratorios, empresas farmacéuticas y países, no nos llevemos a error ¿Adivinan que hizo España?
Responder
28/9/2018 15:41:53
¡Holaaaa Migue! ¡Cuanto tiempo! Que sepas que te tengo "fichado" je,je. Mis tiempos de emular las cabras montesas terminaron, hay muchas maneras de luchar por la naturaleza y mis huesos ya no están para muchos trotes, así que mejor correr un tupido velo.
Responder
Desi Ramos
27/9/2018 02:39:21
Interesante resumen de la vida de este investigador que no conocía a través de su trabajo. He mirado en la Wikipedia y su trabajo lo presentan unido a la investigación de la biología del desarrollo y comprender los mecanismos celulares y moleculares responsables del desarrollo embrionario desde el momento de la fertilización hasta la formación de un organismo, por lo demás solo citan la regeneración de organismos y la lucha contra el envejecimiento ¿apenas hablan de todo esto o no me entero? ¿Es lo mismo?
Responder
28/9/2018 16:13:14
Hola Desideria! Guaaau! como me alegra que te hayas interesado por el tema y te muevas, mis felicidades por tu interés y preguntas (¡menuda batería de cuestiones! ja,ja) Como ya he constestado, tranquila voy a realizar unos reportajes más sobre la edición genética y el ADN de 0 a 100 ...o al menos hasta el 70% ji,ji que no se tanto, vamos (pero tu no lo cuentes). Bueno en serio, otra vez, veo que has entendido la esencia del mecanismo de defensa bacteriano, tus preguntas son más o menos , algunas de las grandes cuestiones de todo esto. Por desgracia la wikipedia no es muy útil para estos temas, aunque es un detalle que al menos hable de Izpisúa como lo que es uno de nuestros grandes investigadores. Verás la carrera de este investigador que comenzó con sus estudios de farmacia precisamente en la ciudad donde transcurre normalmente mi vida: Valencia! es muy larga y su contribución a la biología es increíble! Hablar de todo su trabajo ¡me supondría años! pero solo ahora esta comenzando a ser reconocido a nivel popular por su increíble aportación para mejorar las técnicas que ofrecen las nuevas terapias genéticas y celulares. Pero su trabajo es muy amplio y complejo, cosa que la wiki solo puede resumir. En la wiki hay grandes trabajos sobre genética, pero por desgracia muchos tienen demasiada complejidad para un acercamiento de alguien que se inicia o al reves muy sencillos o con errores, depende quien publique pero en general defiendo la wikipedia como una fuente universal de conocimiento libre a defender.
Responder
Quelecortenlacabeza
30/9/2018 11:05:54
La pregunta que todos hacen se responde rápido: una década, a finales del siglo XX se prometía ya la medicina genética como e futuro, pero fue un espejismo. Han pasado 20 años y se relanzó hace cinco años con CRISPR así que quedan diez, no falla, si me equivoco no serán tres, serán 10. Si hay miles de enfermedades y cada una necesita su cura personalizada y ensayos clínicos ¿Quién paga las pruebas?... igual me he quedado bien corta. Aconsejo ver el documental: Al otro lado del bisturí, nos prometen cosas por dinero, luego no se comprueban bien y llegan las tragedias. ¿Manipular ADN es un fármaco o un dispositivo médico? Porque como sea lo segundo estamos bien listos.
Responder
Padilla
30/9/2018 23:40:19
Aconsejo el video de los dos científicos chinos explicando las herramientas de edición, está hablado en inglés pero si activas los subtitulos te aclaras y da como ternura de los pobrecillos explicando las cosas con objetos normales, me ha enganchado, llamadme friki pero es maravilloso. Chapó con la elección 💪
Responder
Pichi Garrón
3/10/2018 18:57:25
Yo también, ver a los dos genios esos con sus cajitas de "herramientas" da cosilla, pero hace que lo entiendas. Eso sí, por favor, enlacen vídeos en español buenos para estos temas, que seguro que existen, yo busco a veces por Youtube pero no piloto y bajo chorradas, aconsejen por favor.
Responder
25/10/2020 13:57:20
Como comento a Padilla. "Estoy en ello" .Un abrazo 25/10/2020 13:55:51
Tomé nota y estoy en ello desde hace un tiempo, y me apetecía comentarlo para dejar constancia que lo leo todo! y es una buena idea en la que estoy mirando hace un tiempo!
Responder
Deja una respuesta. |