TECNOLOGÍA Y CIENCIA |
|
|
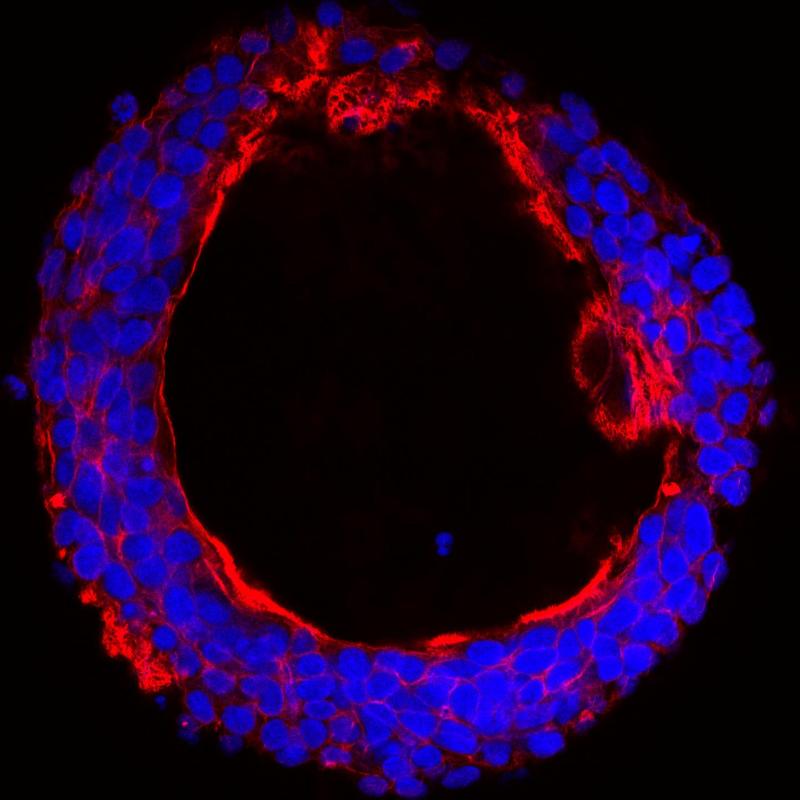
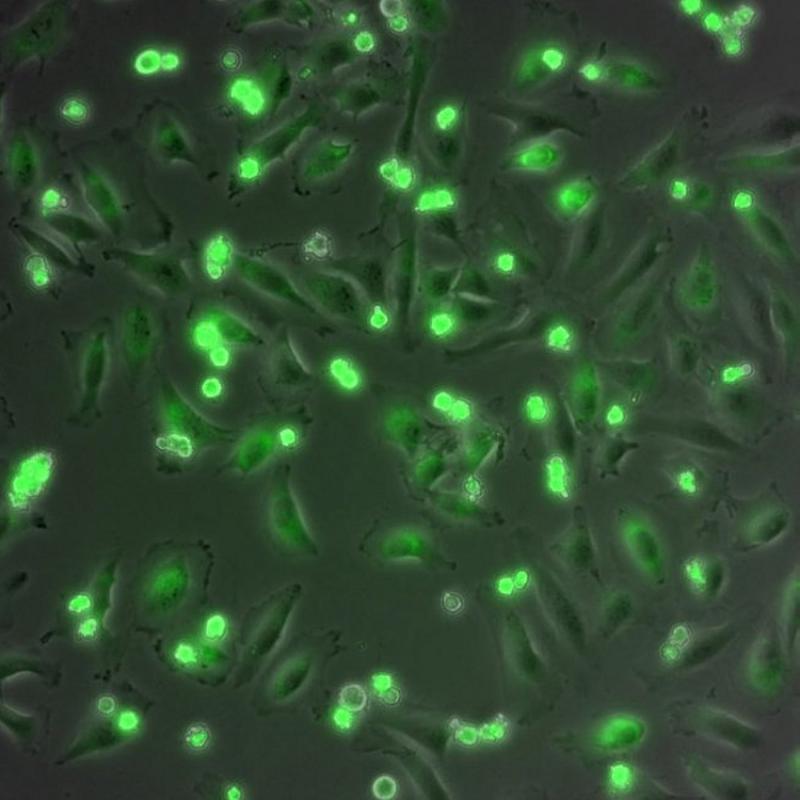
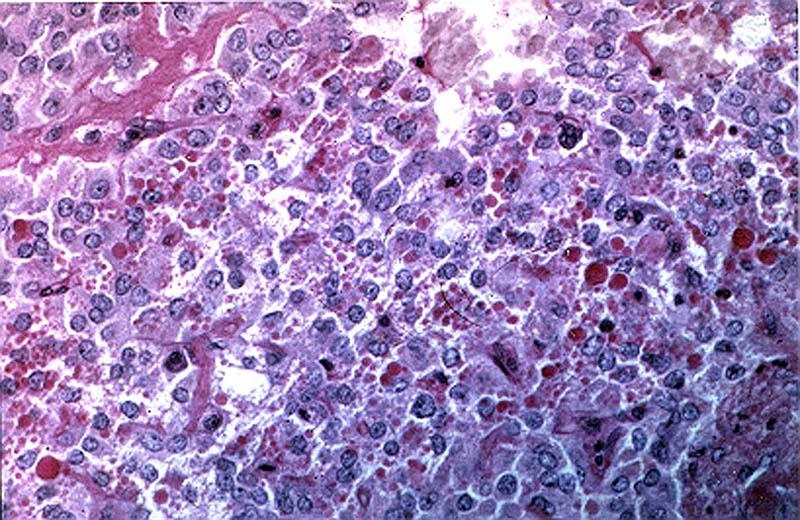
Ya estamos de vuelta este 2018 con nuestros particulares resúmenes temáticos de lo acontecido en el mundo de la ciencia, hoy vamos a comenzar con los últimos hallazgos en la lucha contra el cáncer y que a día de hoy continua imparable en múltiples frentes… Receptor celular en el cáncer de ovario Iniciamos el recorrido muy cerca, con los Investigadores del Grupo de Señalización Molecular en Cáncer, Programa Oncobell del Instituto de Investigación Biomédica de Bellvitge (IDIBELL), del Programa ProCURE del Instituto Catalán de Oncología (ICO) que a principios de año anunciaron la identificación de un receptor celular clave en los procesos de metástasis en cáncer de ovario. El descubrimiento se ha publicado en Molecular Cancer Therapeutics, y gracias a este se da pie a la utilización de inhibidores de este receptor como diana terapéutica en las variantes más agresivas del cáncer de ovario. Desafortunadamente, a día de hoy el diagnóstico del cáncer de ovario suele hacerse muy tardíamente, ya que en el 80% de los casos, los pacientes ya presentan metástasis o diseminaciones peritoneales que pueden afectar a otros órganos vitales. Aunque la combinación de cirugía y quimioterapia con derivados del platino suele ofrecer buenos resultados, el porcentaje de recurrencia de la enfermedad en tan solo dos años es elevado: 70%. Los investigadores de este trabajo consideran el estudio de cómo las células tumorales se diseminan, como básico para entender y mejorar el pronóstico de la enfermedad. Su línea de investigación se ha basado en identificar las moléculas implicadas en esta diseminación, que suele ir acompañada de una acumulación de líquido en la zona del peritoneo (ascitis), y se termina propagando a nivel del torrente sanguíneo. Investigadores del Grupo de Señalización Molecular en Cáncer. A la izquierda la Dra. Agnès Figueras, primera autora del estudio. IDIBELL En el trabajo realizado por el equipo de investigación IDIBELL-ICO se ha conseguido asociar la expresión del receptor CXCR4 en células tumorales de ovario a su potencial de diseminación a través del torrente sanguíneo. CXCR4 es un receptor implicado en el movimiento de las células de la sangre, especialmente en aquellas ubicadas en la médula ósea, que ya había sido relacionado anteriormente con procesos de diseminación en cáncer de mama. En los estudios realizados en modelos ortotópicos los investigadores demostraron que la administración de inhibidores de CXCR4 en aquellos cánceres donde previamente se había detectado la expresión elevada de este receptor, impedía en gran medida la propagación de las células tumorales a nivel sanguíneo y dentro del peritoneo. Paralelamente, también han observado que la eliminación genética de CXCR4 en cultivo celular da lugar a tumores de crecimiento más lento y más bajo porcentaje de diseminación. Precursor de cáncer sanguíneo y riesgo La segunda noticia interesante con la que inauguramos el año, vino el 17 de enero de la Clínica Mayo en Rochester, Minnesota. Los investigadores publicaron en New England Journal of Medicine (Revista de Medicina de Nueva Inglaterra) un estudio donde analizaban como los pacientes con gammapatía monoclonal de significado incierto corren más riesgo de avanzar hacia mieloma múltiple u otro cáncer afín, incluso después de 30 años. En el estudio los investigadores trabajaron con 1384 pacientes y dos tipos principales de gammapatía monoclonal de significado incierto: gammapatía monoclonal de significado incierto tipo IgM y gammapatía monoclonal de significado incierto tipo no IgM. Según el Dr. Vincent Rajkumar, médico hematólogo de Mayo Clinic y autor experto del estudio. La gammapatía monoclonal de significado incierto es una afección en la que se descubre la presencia de una proteína anormal, conocida como proteína monoclonal, en la sangre. Curiosamente, normalmente no causa problemas; pero con el tiempo, puede convertirse en mieloma múltiple, un tipo de cáncer sanguíneo. Dicha enfermedad está presente en más del 3 por ciento de la población general de 50 años o más. En algunos casos, las personas con gammapatía monoclonal de significado incierto avanzan hacia el mieloma múltiple. En el estudio publicado, el Dr. Rajkumar y sus colegas descubrieron que el riesgo general de avanzar hacia el mieloma u otro trastorno afín es relativamente pequeño, de 1 por ciento al año, pero dicho riesgo continúa indefinidamente. También observaron que el riesgo de mieloma u otro cáncer afín era relativamente pequeño, comparado frente a otras causas generales de muerte. Por ello, recomendaron que a los pacientes a quienes se les ofrece seguimiento debido a una gammapatía monoclonal de significado incierto no solo se les revise la presencia o ausencia de algún avance, sino también se les brinde todos los demás servicios preventivos que son habituales en otros pacientes de su misma edad. Así que ya sabemos… en caso de padecer esta dolencia no debemos bajar la guardia incluso pasados 30 años, la mejor parte es que ya sabemos hacia donde avanzará en el futuro: probablemente hacía mieloma múltiple. La enzima “mata-azúcares” que define el cáncer de colon, otro ejemplo de empleo de CRISPR / Cas Los investigadores han identificado una enzima que está ausente en el tejido sano de colon pero abundante en las células de cáncer de colon, según un informe en la edición del 26 de enero de la revista Journal of Biological Chemistry y recogido por EurekAlert! Han observado que la enzima parece conducir la conversión de tejido de colon normal en cáncer mediante la unión de moléculas de azúcar, o glicanos, a ciertas proteínas en la célula. Comprender el papel que juegan las proteínas modificadas con azúcar (glicosiladas) en las células sanas y cancerosas es un área emergente de la biología del cáncer y que podría conducir a nuevas terapias. La enzima GalNAc-T6 está selectivamente regulada en adenocarcinomas de colon, y su expresión se asocia con un patrón de crecimiento similar al cáncer. Kirstine Lavrsen, Universidad de Copenhague El equipo de Hans Wandall en la Universidad de Copenhague estudió un grupo de 20 enzimas que inician el primer paso en un tipo particular de modificación de glucanos, llamada O-glucosilación de tipo GalNAc, que se encuentra en diversas proteínas. Estas enzimas, llamadas GalNAc transferasas (GalNAc -Ts) se encuentran de diversas maneras en diferentes cantidades en diferentes tejidos, pero sus funciones son poco conocidas. El equipo de Wandall, dirigido por la estudiante de posgrado Kirstine Lavrsen, descubrió que una de las GalNAc-Ts, llamada GalNAc-T6, estaba ausente en el tejido sano de colon pero abundante en células de cáncer de colon. El equipo utilizó la ingeniería CRISPR / Cas de una línea celular de cáncer de colon con y sin GalNAc-T6 para comprender a qué proteínas la enzima ayudaba a unir azúcares y qué efecto tenía en las células. "Cuando vemos el crecimiento 3D de una línea celular cancerosa que tiene GalNAc-T6, observamos que puede formar estructuras tubulares con la formación de algo que se parece al tejido del cáncer de colon", explica Wandall. "Cuando sacamos GalNAc-T6, de repente la formación de tejido cambia para parecerse más a las estructuras de las zonas que se encontrarían en un colon saludable". Usando espectrometría de masas, el equipo clasificó las proteínas sobre las que actuaba GalNAc-T6 en estas células, los resultados sugieren que esta enzima específica parece afectar un subconjunto de proteínas que podrían estar involucradas en la adhesión célula-célula". En otras palabras: las modificaciones del glucano cambiaron los patrones en los que las células se unían, lo que hace que las células se desarrollen como algo que se parece más a un tumor que a un tejido sano. El siguiente paso, entonces, es comprender con precisión por qué el agregado de azúcares a los sitios proteínicos específicos modificados por GalNAc-T6 lleva a que las células del colon se desarrollen anormalmente. Las modificaciones de glucano pueden afectar la función de la proteína en innumerables formas. Por ejemplo, pueden hacer que las proteínas que generalmente se dividen en dos no puedan dividirse, o evitar que dos proteínas se unan entre sí. Wandall espera que la comprensión de la glucosilación en las células cancerígenas conduzca a mejores herramientas de diagnóstico temprano, medicamentos o inmunoterapias. "Los glicanos agregan una capa de contexto adicional que podría ayudarnos a crear intervenciones más específicas", explica Wandall. "Los glicanos se ven tan diferentes en el cáncer en comparación con el tejido normal, y es un campo realmente poco estudiado", dijo Lavrsen. "Hay muchas cosas por descubrir". El número de mitocondrias y la resistencia a la quimioterapia: Terapias más ajustadas al paciente Siguiendo con la lucha contra el cáncer, vamos a centrarnos en un estudio sobre uno de los tratamientos más comunes y la resistencia de las células malignas. Un estudio publicado en enero en la revista Nature Communications, explica según sus autores, científicos del CNB, de la Universidad Autónoma de Madrid y los hospitales de Torrevieja y Vinalopó (Alicante), por qué algunas células mueren tras el tratamiento antitumoral mientras otras, genéticamente idénticas, son capaces de sobrevivir y causar la reaparición del cáncer. Células Hela, donde las mitocondrias se han teñido en verde; se obtuvo tras 12 horas de exposición al agente quimioterapéutico TRIAL. Las células muertas (más redondeadas) muestran una mayor cantidad de mitocondrias que las células vivas. Francisco Iborra, CNB-CSIC. Los investigadores españoles han constatado que el número de mitocondrias de una célula tumoral predice su sensibilidad a la quimioterapia, siendo aquellas que tienen un elevado número de mitocondrias las que responden bien al tratamiento. Por lo que el número de dichas mitocondrias podría servir para predecir la sensibilidad del paciente a un determinado tratamiento, suponiendo un cambio frente a lo pensado hasta ahora, donde las diferencias de sensibilidad a la quimioterapia se habían asociado a las variaciones genéticas. Según explica Francisco Iborra, director del trabajo e investigador del CNB-CSIC, “No todo es determinado por la genética, el contexto interno y externo influye profundamente en la célula”. El estudio comprueba que las variaciones en la cantidad de mitocondrias pueden ser la causa de la diferente sensibilidad de células genéticamente idénticas al mismo tratamiento antitumoral. El Centro Nacional de Biotecnología del Consejo Superior de Investigaciones Científicas (CNB-CSIC) publicó una nota de prensa donde recuerda que uno de los grandes problemas de los tratamientos de quimioterapia es la resistencia que presentan algunos pacientes debido a que la terapia no es eficaz contra todas las células tumorales, ya que algunas sobreviven y siendo capaces de regenerar el tumor. Este nuevo estudio podría ofrecer nuevas herramientas a la hora de elegir qué terapia asignar a un determinado paciente, Francisco Iborra lo aclara: “Hasta la fecha, carecíamos de biomarcadores que nos sirvieran para predecir la respuesta de las células tumorales a los tratamientos convencionales; creemos que la masa mitocondrial podría ser un buen indicador de prognosis y predecir si un tratamiento será efectivo ante un determinado cáncer” . Las mitocondrias, que podríamos decir que son las fábricas de energía de las células de organismos superiores, no es igual en todas las células si no que depende del reparto o durante la división celular. Los resultados muestran que las células con más mitocondrias presentan mayor cantidad de proteínas apoptóticas, es decir inductoras de la muerte celular, así, las células con alto contenido mitocondrial son más propensas a morir a causa de fármacos antitumorales. Así pues, el análisis de las biopsias de cáncer de colon que se han realizado para poder realizar este estudio apoya la hipótesis de la correlación entre la masa mitocondrial y las proteínas que inducen la muerte de la célula. Ahora que se ha comprobado con biopsias de cáncer de colon, comienza una segunda fase para validar los resultados con muestras de diferentes tumores y con diferentes fármacos, para comprobar si estas observaciones son extrapolables abriendo un nuevo camino, a la hora de personalizar los tratamientos de quimioterapia a los distintos pacientes tras comprender mejor porque las células tumorales de algunos pacientes son más resistentes a los tratamientos. Nueva estrategia terapéutica potencial para el cáncer de páncreas Continuamos ahora por el frente de los nuevos tratamientos contra uno de los cánceres más letales y difíciles de tratar: el cáncer de páncreas. A principios de febrero, investigadores del CNIO han presentado una nueva estrategia terapéutica potencial para esta letal variante del cáncer. Los científicos liderados por Magdolna Djurec primera autora del trabajo y Carmen Guerra, una de las principales investigadoras, han publicado en la revista Proceedings of the National Academy of Science (PNAS), un estudio donde informan de cómo han aislado una subpoblación de fibroblastos asociados al cáncer, que promueven el crecimiento tumoral, descubriendo que el gen Saa3 es al menos uno de los genes responsables de la propiedad que fomenta el crecimiento tumoral en estas células. Tumor sólido-pseudopapilar de páncreas. Las células tumorales contienen núcleos ovales o redondos con nucleolo prominente, mostrando un citoplasma eosinófilo de moderado tamaño. J. Azúa-Romeo Desafortunadamente, en la mayoría de los pacientes con cáncer de páncreas, el diagnóstico se realiza cuando la enfermedad ya está avanzada y no hay un tratamiento efectivo posible. Pese a los esfuerzos de muchos investigadores, en las últimos años no ha habido logros significativos para combatirlo, lamentablemente, su ocurrencia está en aumento. Ahora, un grupo de investigadores del Centro Nacional de Investigaciones Oncológicas (CNIO) de España podría haber encontrado una nueva forma de ataque que abre la puerta al diseño de futuras estrategias terapéuticas, aunque todavía es demasiado pronto para pensar en su uso clínico. El cáncer de páncreas se caracteriza por que las células tumorales están incrustadas en el estroma, el cual representa el 90% de la masa tumoral y que actúa como una barrera (física y química) que dificulta el tratamiento con inhibidores, quimioterapia e inmunoterapia. La mayor parte de los estudios realizados hasta la fecha se han centrado principalmente en las células tumorales, mientras que las células que forman el estroma siguen siendo un misterio, a pesar de los diferentes equipos de investigadores han observado a lo largo del tiempo que algunos componentes del estroma promueven la progresión tumoral. Hace poco tiempo, varios de estos grupos de investigadores interesados por el estroma trataron de eliminar las células más abundantes que hay en este, los llamados fibroblastos asociados al cáncer (CAF), pero sin embargo lograron el efecto contrario al esperado: el tumor continuó progresando con una agresividad todavía mayor, por lo que se supuso de este resultado que algunas de las células eliminadas podían tener funciones antitumorales. Así pues, los investigadores del Grupo de Oncología Experimental del CNIO enfocaron su trabajo en la búsqueda de una población de células estromales que fomentara el crecimiento tumoral y una vez identificadas averiguar por qué tienen esa propiedad concreta y revertirla. Para conseguir esto han diseñado un método innovador porque en lugar de eliminar estas células que ayudan al progreso del tumor, su objetivo ha consistido en la reprogramación selectiva de dichas células del estroma. Los investigadores se centraron en una subpoblación de fibroblastos que se sabe que desempeñan un papel en la inflamación, la cual fomenta el crecimiento tumoral. La primera fase consistió en analizar todos los genes que se expresan diferencialmente en los fibroblastos estromales del tumor, los CAF, en comparación con los fibroblastos del tejido pancreático sano. La hipótesis planteada era que los posibles genes responsables del papel pro tumoral de los CAF se expresarían en altos niveles solo en estos fibroblastos, y no en fibroblastos del tejido sano. La investigación mostró que el gen Saa3 es responsable de los CAF que ayudan al progreso de las células tumorales. Cuando los investigadores eliminaron la expresión de este gen en los CAF, estas células se comportaron como fibroblastos normales, al perder la capacidad de ayudar al progreso de las células tumorales, es decir lograron "reprogramar" estas células, al eliminar sus propiedades pro tumorales. Así pues, este descubrimiento podría ayudar a nuevas estrategias terapéuticas combinándose con inmunoterapia, quimioterapia o inhibidores contra rutas de señalización específicas de las células tumorales y abre la puerta a nuevas investigaciones en muchos laboratorios destinados a reprogramar el estroma en lugar de eliminarlo. Esta investigación es probablemente la primera de otras, porque los investigadores todavía siguen estudiando el papel de otros genes de relevancia potencial que se encuentran en el análisis de expresión comparativa de los fibroblastos estromales del tumor. El equipo comenzó este complejo trabajo en el año 2011, en un tremendo juego de equipo donde el Grupo de Oncología Experimental del CNIO ha trabajado con expertos en bioinformática del CNIO y el grupo de Raul Rabadan en la Universidad de Columbia, en Nueva York, así como el grupo de Andreas Trumpp en el Centro Alemán de Investigación del Cáncer (DKFZ), en Heidelberg, y el grupo de Bruno Sainz Jr. en Universidad Autónoma de Madrid (UAM), que participa con el Grupo de Oncología Experimental en un proyecto AECC. Por último, las muestras tumorales en pacientes humanos se obtuvieron gracias a la inestimable colaboración con el cirujano Francisco Sánchez-Bueno del Hospital Arritxaca de Murcia, España. Rubén Luna S.
Temas relacionados: Divulgación científica, Biomedicina, Rubén Luna S, Medicina. Reconocimientos y más información sobre la obra gráfica ADVERTENCIA: En este foro, no se admitirán por ninguna razón el lenguaje soez y las descalificaciones de ningún tipo. Se valorará ante todo la buena educación y el rigor sobre el tema a tratar, así que nos enorgullece reconocer que rechazaremos cualquier comentario fuera de lugar.
0 Comentarios
Deja una respuesta. |